题目内容
在一个密闭的容器中有氧气、二氧化碳、水蒸气和一种未知物W,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,则下列说法中正确的是( )
| 物 质 | 氧 气 | 二氧化碳 | 水蒸气 | W |
| 反应前质量/g | 50 | 5 | 6 | 16 |
| 反应后质量/g | x | 27 | 24 | 0 |
| A、反应后x的值是24 |
| B、反应生成二氧化碳与水的质量比为9:8 |
| C、16gW中含有氢元素1g |
| D、物质W中含有碳、氢、氧三种元素 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律的质量守恒,结合表格中的数据,可推测x的值;根据物质的质量增加或减少,可判断其为反应物还是生成物.
解答:解:根据质量守恒定律:50+5+6+16=x+27+24+0,则x=26,则可知反应物为:氧气、W;生成物为二氧化碳与水蒸气.二氧化碳中的碳元素的质量为22g×
×100%=6g,水中的氢元素的质量为18g×
×100%=2g,6g+2g=8g,小于16g,故W含有碳、氢、氧元素.
A、根据质量守恒定律,x的值为26,故A错误;
B、反应生成二氧化碳与水的质量比为22g:18g=11:9,故B错误;
C、根据质量守恒定律,16gW中含有氢元素2g,故C错误;
D、反应物W中含有碳、氢、氧三种元素,故D正确.
故选D.
| 12 |
| 44 |
| 2 |
| 18 |
A、根据质量守恒定律,x的值为26,故A错误;
B、反应生成二氧化碳与水的质量比为22g:18g=11:9,故B错误;
C、根据质量守恒定律,16gW中含有氢元素2g,故C错误;
D、反应物W中含有碳、氢、氧三种元素,故D正确.
故选D.
点评:掌握质量守恒定律的内容:在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案
相关题目
已知Si+2NaOH+H2O═Na2SiO3+2H2↑;2Al+2NaOH+2H2O═2NaAlO2+3H2↑ 硅不与盐酸反应,镁不与碱反应.将含镁硅铝的合金样品分为等质量的两份,分别与足量的稀盐酸和烧碱溶液反应,测得放出的氢气质量相同.则该合金样品中镁硅铝的质量比不可能是( )
| A、12:7:54 |
| B、24:28:54 |
| C、24:14:54 |
| D、48:28:27 |
下列化学方程式不能用离子方程式Ba2++SO42-═BaSO4↓表示的是( )
| A、Ba(NO3)2+H2SO4═BaSO4↓+2HNO3 |
| B、BaCl2+Na2SO4═BaSO4↓+2NaCl |
| C、BaCl2+H2SO4═BaSO4↓+2HCl |
| D、BaCO3+H2SO4═BaSO4↓+H2O+CO2↑ |
如图所示的四个实验,其中没有发生化学变化的是( )
A、 电解水 |
B、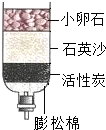 水的净化 |
C、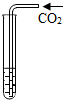 二氧化碳通入蒸馏水中 |
D、 水滴入装有生石灰的试管中 |
碳的耗损量叫做“碳足迹”,一般情况下,损耗的二氧化碳量越大,“碳足迹”就越大,以下做法可以减少“碳足迹”的是( )
| A、以自行车代替汽车出行 |
| B、大量使用煤、石油等燃料 |
| C、将生活垃圾焚烧处理 |
| D、大量使用一次性木筷 |
下列物质“一定”的说法中正确的是( )
| A、由同种元素组成的物质一定是单质 |
| B、纯净物一定是由同种元素组成的 |
| C、纯净物一定是由同种分子构成的物质 |
| D、化合反应的生成物一定是化合物 |
下列各组变化中均属于化学变化的一组是( )
| A、铁生锈,水结冰,钢锭抽成丝 |
| B、蜡烛熔化,镁燃烧,玻璃破碎 |
| C、碳燃烧,车胎放炮,木材造船 |
| D、煤燃烧,石灰水变浑,石灰石煅烧生石灰 |
物质的性质决定物质的用途,以下用途利用其化学性质的是( )
| A、用石墨做铅笔芯 |
| B、镁粉用做烟火和照明弹 |
| C、干冰用于人工降雨 |
| D、铜丝用做电线 |