题目内容
菱铁矿的主要成分是FeCO3.下列说法正确的是( )A.FeCO3中Fe、C、O元素的质量比是1:l:3
B.FeCO3中Fe、C、O的原子个数比是56:12:16
C.FeCO3的相对分子质量是56+12+16
D.FeCO3中Fe元素的质量分数是
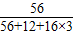 ×100%
×100%
【答案】分析:A、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
B、根据化学式右下角的数字确定物质中个元素的原子个数比
C、相对分子质量;是各元素的相对原子质量的总和
D、根据物质中某元素的质量分数= ×100%,进行解答.
×100%,进行解答.
解答:解:A、FeCO3中铁、碳、氧元素的质量比为:56:12:(16×3)=14:3:12;故错
B、根据化学式FeCO3Fe、C、O的元素的原子个数比为:1:1:3;故错
C、FeCO3的相对分子质量为:56+12+16×3=116;故错
D、FeCO3中Fe元素的质量分数为: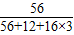 ×100%.故对
×100%.故对
故选D
点评:本题主要考查学生根据化学式确定物质元素及根据组成物质元素之间的质量关系进行分析解题的能力.
B、根据化学式右下角的数字确定物质中个元素的原子个数比
C、相对分子质量;是各元素的相对原子质量的总和
D、根据物质中某元素的质量分数=
 ×100%,进行解答.
×100%,进行解答.解答:解:A、FeCO3中铁、碳、氧元素的质量比为:56:12:(16×3)=14:3:12;故错
B、根据化学式FeCO3Fe、C、O的元素的原子个数比为:1:1:3;故错
C、FeCO3的相对分子质量为:56+12+16×3=116;故错
D、FeCO3中Fe元素的质量分数为:
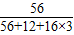 ×100%.故对
×100%.故对故选D
点评:本题主要考查学生根据化学式确定物质元素及根据组成物质元素之间的质量关系进行分析解题的能力.

练习册系列答案
相关题目
(1)请用横线将下列金属的性质与它适合制造的对象连接起来:
制造电灯丝的金属 硬度大
做切割工具用的金属 熔点高
制造保险丝的金属 耐腐蚀
制造医疗器械的金属 熔点低
从连线中你可以获得一些规律或感悟,请写出一点________
(2)制取合金常用的方法是将两种或多种金属(或金属与非金属)加热到某一温度,使其全部熔化,再冷却成为合金.根据下表中的数据判断(其他条件均满足),下列合金不宜采用上述方法制取的是________
| 金 属 | Na | Mg | Al | Cu | Fe |
| 熔点(℃) | 97.5 | 649 | 660 | 1083 | 1535 |
| 沸 点(℃) | 883 | 1090 | 2467 | 2567 | 2750 |
(3)工业上把能用来提炼金属的矿物叫做矿石.赤铁矿的主要成分是氧化铁、菱铁矿的主要成分是碳酸亚铁,请写出这两种矿石主要成分的化学式________、________,鉴别这两种矿石可以用试剂________,通过观察________来鉴别.
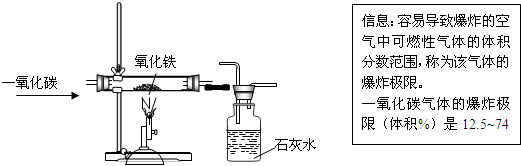
(4)把铁矿石炼成铁是一个复杂的过程.实验室仿照其原理做下列实验
a.写出实验中的反应现象________
b.用化学方程式表示实验图中发生的化学变化________
c.指出该装置的不妥之处,说明原因并提出改进措施________
d.阅读右侧信息后你认为要安全成功地完成实验,必须进行的操作要求是________.