题目内容
15.将镁和氧化镁的混合物3.2g,加入到98g质量分数为10%的稀硫酸中,恰好完全反应,则所得溶液中溶质的质量为( )| A. | 6.4g | B. | 8.1g | C. | 10g | D. | 12g |
分析 根据镁和硫酸反应生成硫酸镁和氢气,氧化镁和硫酸反应生成硫酸镁和水,所以反应后的溶液中的溶质是硫酸镁,然后依据硫酸根离子守恒进行计算.
解答 解:设反应后所得溶液中溶质的质量为x
S${{O}_{4}}^{2-}$-------MgSO4,
96 120
98g×10%×$\frac{96}{98}$ x
$\frac{96}{98g×10%×\frac{96}{98}}$=$\frac{120}{x}$
x=12g
故选:D.
点评 本题考查学生应用元素、离子守恒的方法来计算是解答中的关键,不可盲目利用化学方程式来计算.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.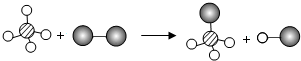 某化学反应的微现示意图如图所示(不同小球代表不同的原子).关于该图说法下列错误的是( )
某化学反应的微现示意图如图所示(不同小球代表不同的原子).关于该图说法下列错误的是( )
 某化学反应的微现示意图如图所示(不同小球代表不同的原子).关于该图说法下列错误的是( )
某化学反应的微现示意图如图所示(不同小球代表不同的原子).关于该图说法下列错误的是( )| A. | 反应前后共有四种分子 | B. | 反应前后分子没有变化 | ||
| C. | 反应前后原子没有变化 | D. | 反应前后原子的组合方式发生变化 |
10.属于浊液的是( )
| A. | 糖水 | B. | 盐水 | C. | 油水 | D. | 汽水 |
4.下列是几种粒子的结构示意图,有关说法不正确的是( )

| A. | ①和②属同种元素 | B. | ④属于金属元素 | ||
| C. | ①和③的化学性质相似 | D. | ②化学性质稳定,属于稀有气体元素 |
5.如图所示实验操作正确的是( )
| A. |  点燃酒精灯 | B. |  检查装置的气密性 | ||
| C. |  读出液体的体积 | D. |  液体的取用 液体的取用 |
 钠的化合物是中学化学学习和研究的重要内容.
钠的化合物是中学化学学习和研究的重要内容.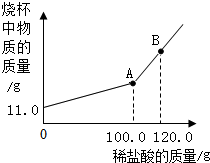 我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献.
我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献.