题目内容
3. 我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献.
我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献.(1)主产品Na2CO3的俗名是纯碱或苏打,副产品氯化铵中阳离子符号为NH4+.
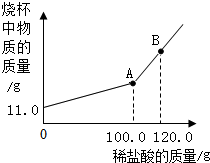
(2)在实际生产中,产品Na2CO3中常混有少量的NaCl,现有样品11.0g,将其放入干净的烧杯中,向烧杯中逐滴加入溶质质量分数为7.3%的稀盐酸,反应后烧杯中物质的质量与滴入稀盐酸的质量关系如图所示.
①图中A点表示Na2CO3与盐酸或HCl恰好完全反应,B点的溶质为NaCl、HCl.
②计算样品中Na2CO3的质量分数(计算结果精确至0.1%)
分析 (1)根据碳酸钠的俗名和氯化铵的构成分析回答;
(2)根据图象溶液的总质量与加入的稀盐酸的关系分析碳酸钠与稀盐酸的反应,当滴加稀盐酸溶液至图中A点时氯化钠与稀盐酸恰好反应,可以计算溶质的质量,即可求出样品中Na2CO3的质量分数;当在B点时,稀盐酸是过量的,据此分析溶液中的溶质.
解答 解:(1)主产品Na2CO3的俗名是纯碱或苏打,副产品氯化铵中阳离子是铵根离子,符号为NH4+.
(2))①由图象可知,当滴入上述稀盐酸至图中A点时,加入的稀盐酸恰好与碳酸钠反应.由图象可知,当滴入上述稀盐酸至图中B点时,加入的稀盐酸的量是过量的,烧杯中溶液里的溶质为NaCl、HCl.
设样品中,含Na2CO3的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73
x 100g×7.3%
$\frac{106}{x}=\frac{73}{100g×7.3%}$ 解得::x=10.6g
②样品中Na2CO3的质量分数是:$\frac{10.6g}{11g}×100%$≈96.4%
故答为:(1)纯碱或苏打,NH4+;(2)①Na2CO3与盐酸或HCl恰好完全反应,NaCl、HCl;②样品中Na2CO3的质量分数为96.4%.
点评 本题属于图象题,解题的关键是根据图象中量的变化关系,分析出反应进行的情况,从而进行有关的分析与计算.

练习册系列答案
相关题目
13.等质量的质量分数均为4%的氢氧化钠溶液与稀盐酸充分反应,所得溶液呈( )
| A. | 碱性 | B. | 酸性 | C. | 中性 | D. | 无法判断 |
18.将24g含有小苏打的胃药(杂质不溶于水,也不与酸反应)加入烧杯中,向其中加入l00g 质量分数10.95%的稀盐酸充分反应,过滤,得到108g滤液,则该胃药中主要成分的质量分数为( )
| A. | 80% | B. | 70% | C. | 87.5% | D. | 90% |
15.将镁和氧化镁的混合物3.2g,加入到98g质量分数为10%的稀硫酸中,恰好完全反应,则所得溶液中溶质的质量为( )
| A. | 6.4g | B. | 8.1g | C. | 10g | D. | 12g |
12.分析类比和推理是化学学习的思维方式.下列分析、类比和推理正确的是( )
| A. | 浓硫酸具有吸水性,所以浓盐酸也具有吸水性 | |
| B. | 在化学反应中,质量和化学性质都不改变的物质一定是催化剂 | |
| C. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| D. | 组成CO和CO2的元素相同,但它们的分子构成不同,所以它们的化学性质不同 |
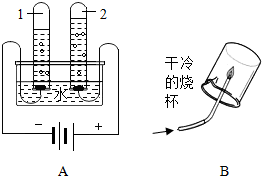 研究物质的组成是化学学科的人物之一.
研究物质的组成是化学学科的人物之一.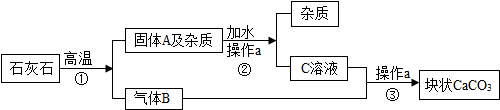
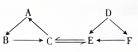 如图所示A~F是初中化学常见的物质,图中“→“表示转化关系.其中A、B、C三种物质都是化合物,且A是一种氧化物.它们都含有钙元素;D、E、F三种物质的组成元素中一种是相同的.E能使澄清石灰水变浑浊.
如图所示A~F是初中化学常见的物质,图中“→“表示转化关系.其中A、B、C三种物质都是化合物,且A是一种氧化物.它们都含有钙元素;D、E、F三种物质的组成元素中一种是相同的.E能使澄清石灰水变浑浊.