题目内容
在学习中我们了解到常用制取氧气的方法有如图所示的四种:请回答问题:

(1)工业上常采用途径丁来制取氧气,这种方法是 (填“物理”或“化学”)变化.以绿色化学的理念,你认为甲、乙、丙三种制取氧气的途径中, (填“甲”、“乙”或“丙”)途径更能体现化学实验的绿色化追求.
(2)下列是实验室制取氧气的一些装置,请回答有关问题
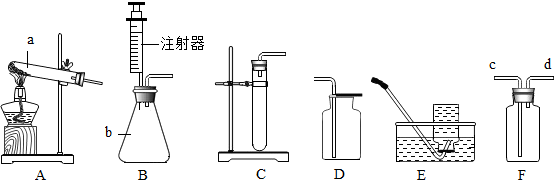
①写出 a、b仪器的名称:a ,b .
②实验室采用途径甲制取氧气,应选用的发生装置是 (填编号),试管口要放 ,目的是 ,该反应的化学方程式是 ,基本反应类型是 .
③采用途径乙制取氧气的化学方程式是 ,如需随时控制生成气体的量并节约药品,发生装置最好选用 (填编号),如用D装置收集氧气,检验氧气是否收集满的方法是 .
④F装置中充满水时,也可以作为氧气的收集装置,则氧气应从 (填“c”或“d”) 端通入.

(1)工业上常采用途径丁来制取氧气,这种方法是
(2)下列是实验室制取氧气的一些装置,请回答有关问题

①写出 a、b仪器的名称:a
②实验室采用途径甲制取氧气,应选用的发生装置是
③采用途径乙制取氧气的化学方程式是
④F装置中充满水时,也可以作为氧气的收集装置,则氧气应从
考点:氧气的制取装置,氧气的工业制法,氧气的收集方法,氧气的检验和验满,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据工业上分离液态空气制取氧气是利用液态氧和液态氮的沸点不同而分离出氧气分析变化;
(2)甲、乙、丙三种制取氧气的途径中,加热氯酸钾和二氧化锰或加热高锰酸钾制取氧气需要加热,浪费能源还污染环境,过氧化氢制取氧气,装置操作简单、安全,不需加热,生成物是水和氧气,无污染,据此分析;根据用加热高锰酸钾的方法制取氧气的发生装置和反应条件选择发生装置;根据加热高锰酸钾时的注意事项分析试管口的处理;根据排水法收集气体的注意事项分析;验满氧气的方法是将带火星的木条放于集气瓶口,看能否复燃;根据氧气不易溶于水,分析进气口.
(2)甲、乙、丙三种制取氧气的途径中,加热氯酸钾和二氧化锰或加热高锰酸钾制取氧气需要加热,浪费能源还污染环境,过氧化氢制取氧气,装置操作简单、安全,不需加热,生成物是水和氧气,无污染,据此分析;根据用加热高锰酸钾的方法制取氧气的发生装置和反应条件选择发生装置;根据加热高锰酸钾时的注意事项分析试管口的处理;根据排水法收集气体的注意事项分析;验满氧气的方法是将带火星的木条放于集气瓶口,看能否复燃;根据氧气不易溶于水,分析进气口.
解答:解:
(1)工业上分离液态空气制取氧气,根据液态氧和液态氮的沸点不同而分离出氧气,所以是物理变化;甲、乙、丙三种制取氧气的途径中,加热氯酸钾和二氧化锰或加热高锰酸钾制取氧气需要加热,浪费能源还污染环境,过氧化氢制取氧气,装置操作简单、安全,不需加热,生成物是水和氧气,无污染,更能体现化学实验的绿色化追求;
(2)①a是试管,b是锥形瓶;
②用加热高锰酸钾的方法制取氧气选用固体加热型的发生装置A;加热高锰酸钾时要在试管口放一团棉花,防止高锰酸钾粉末进入导管;为了收集纯净的氧气,要等气泡连续且均匀冒出时才开始收集;该反应的符号表达式是:2KMnO4
K2MnO4+MnO2+O2↑;该反应是一种物质生成三种物质的分解反应;
③过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,该反应的符号表达式是:2H2O2
2H2O+O2↑;用注射器可以控制液体的滴加速率,因此随时控制生成气体的量并节约药品,应该选择B装置;用向上排空气法收集氧气验满的方法是:将带火星的木条放于集气瓶口,若木条复燃则收集满了;因为氧气不易溶于水,因此应该从短管进入,利用气压把水压出,收集到氧气,即从d管进入;
故答案为:
(1)物理;乙;
(2)①试管;锥形瓶;
②A; 一团棉花;防止高锰酸钾粉末进入导管;导管口连续均匀放出气泡; 2KMnO4
K2MnO4+MnO2+O2↑; 分解反应;
③2H2O2
2H2O+O2↑;B;将带火星的木条放于集气瓶口,若木条复燃则收集满了;
④d.
(1)工业上分离液态空气制取氧气,根据液态氧和液态氮的沸点不同而分离出氧气,所以是物理变化;甲、乙、丙三种制取氧气的途径中,加热氯酸钾和二氧化锰或加热高锰酸钾制取氧气需要加热,浪费能源还污染环境,过氧化氢制取氧气,装置操作简单、安全,不需加热,生成物是水和氧气,无污染,更能体现化学实验的绿色化追求;
(2)①a是试管,b是锥形瓶;
②用加热高锰酸钾的方法制取氧气选用固体加热型的发生装置A;加热高锰酸钾时要在试管口放一团棉花,防止高锰酸钾粉末进入导管;为了收集纯净的氧气,要等气泡连续且均匀冒出时才开始收集;该反应的符号表达式是:2KMnO4
| ||
③过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,该反应的符号表达式是:2H2O2
| ||
故答案为:
(1)物理;乙;
(2)①试管;锥形瓶;
②A; 一团棉花;防止高锰酸钾粉末进入导管;导管口连续均匀放出气泡; 2KMnO4
| ||
③2H2O2
| ||
④d.
点评:本考点主要考查气体的制取装置和收集装置的选择,同时也考查了仪器的名称、文字表达式的书写和催化剂的探究等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
在1个H2SO4和1个H3PO4分子中,不正确的是( )
| A、氧元素的质量分数一样 |
| B、氧原子个数一样多 |
| C、其相对分子质量一样 |
| D、硫元素和磷元素的个数一样多 |



 有六种途径可以制得氧气,如图所示:
有六种途径可以制得氧气,如图所示: