题目内容
某校化学兴趣小组的同学开展了测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验.他们设计了如下的实验方案:

(1)“操作1”的名称是 ,溶液M中的溶质 (写化学式).
(2)滴加CaCl2溶液应“过量”,否则会使测定的结果 (填“偏大”或“偏小”),确定CaCl2溶液是否过量的方法是 .
(3)该混合物中Na2CO3的质量分数是多少?(写出解题过程,计算结果精确到0.1%)

(1)“操作1”的名称是
(2)滴加CaCl2溶液应“过量”,否则会使测定的结果
(3)该混合物中Na2CO3的质量分数是多少?(写出解题过程,计算结果精确到0.1%)
考点:实验探究物质的组成成分以及含量,过滤的原理、方法及其应用,盐的化学性质,根据化学反应方程式的计算
专题:科学探究
分析:(1)根据碳酸钠溶液和氯化钙溶液反应生成碳酸钙沉淀和氯化钠,过滤可用于难溶性固体物质的分离进行解答;
(2)根据加入的CaCl2溶液的量不足时,得到的沉淀量会偏小,氯化钙溶液能和碳酸钠反应生成碳酸钙沉淀进行解答;
(3)根据碳酸钙的质量求出碳酸钠的质量,进而求出该混合物中Na2CO3的质量分数即可.
(2)根据加入的CaCl2溶液的量不足时,得到的沉淀量会偏小,氯化钙溶液能和碳酸钠反应生成碳酸钙沉淀进行解答;
(3)根据碳酸钙的质量求出碳酸钠的质量,进而求出该混合物中Na2CO3的质量分数即可.
解答:解:(1)碳酸钠溶液和氯化钙溶液反应生成碳酸钙沉淀和氯化钠,过滤可用于难溶性固体物质的分离,所以“操作1”的名称是过滤,由于氯化钙溶液过量,所以溶液M中的溶质是氯化钠和氯化钙;故填:过滤;NaCl、CaCl2;
(2)加入的CaCl2溶液的量不足时,得到的沉淀量会偏小,所以滴加CaCl2溶液应“过量”,否则会使测定的结果偏小;氯化钙溶液能和碳酸钠反应生成碳酸钙沉淀,所以确定CaCl2溶液是否过量的方法是取少量溶液M,滴入适量的碳酸钠,若有沉淀产生,则CaCl2溶液过量;故填:偏小;取少量溶液M,滴入适量的碳酸钠,若有沉淀产生,则CaCl2溶液过量;
(3)设混合物中碳酸钠的质量为x.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10g
=
x=10.6g
该混合物中Na2CO3的质量分数=
×100%=96.4%
答:该混合物中Na2CO3的质量分数为96.4%.
(2)加入的CaCl2溶液的量不足时,得到的沉淀量会偏小,所以滴加CaCl2溶液应“过量”,否则会使测定的结果偏小;氯化钙溶液能和碳酸钠反应生成碳酸钙沉淀,所以确定CaCl2溶液是否过量的方法是取少量溶液M,滴入适量的碳酸钠,若有沉淀产生,则CaCl2溶液过量;故填:偏小;取少量溶液M,滴入适量的碳酸钠,若有沉淀产生,则CaCl2溶液过量;
(3)设混合物中碳酸钠的质量为x.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10g
| 106 |
| x |
| 100 |
| 10g |
x=10.6g
该混合物中Na2CO3的质量分数=
| 10.6g |
| 11g |
答:该混合物中Na2CO3的质量分数为96.4%.
点评:此题涉及到实验的常规操作,相关的物质的分离设计了三种方式,纵纵观这些方式实际还是与物质之间的反应有关系,因此学好物质间的联系是酸碱盐知识的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列例举的是生活中常见的物质的pH,你认为数据不合理的是( )
| A、橙汁pH=4 |
| B、胃液pH=12 |
| C、肥皂水pH=11 |
| D、食醋pH=3 |
今年冬季,雾霆天气笼罩了我国中东部大部分地区,其中二氧化硫、氮氧化物和可吸入颗粒物(如PM2.5等)是形成雾霆的主要原因.下列措施可以有效遏制雾霾形成的是( )
| A、加高工厂烟囱 |
| B、推进汽车油品升级,减少有害物质排放 |
| C、大力发展火力发电 |
| D、建筑工地扬尘施工最好在夜间 |
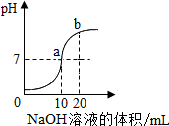 数字化装备正逐步进入宜昌市的各个校园.在盐酸和氢氧化钠反应的过程中,如图是利用数字化传感器得到的溶液pH变化图象.
数字化装备正逐步进入宜昌市的各个校园.在盐酸和氢氧化钠反应的过程中,如图是利用数字化传感器得到的溶液pH变化图象.
 二氧化碳在生产生活中有着广泛的应用.
二氧化碳在生产生活中有着广泛的应用.