题目内容
4.在学过酸碱能发生中和反应后,王彤昊同学和韩睿宇同学对实验中所加入试剂的顺序等相关问题产生了疑问,请你和他们一起来回答下列问题:【1】王彤昊同学直接向盛有少量氢氧化钠溶液的烧杯中加入一定量稀盐酸,结果没有产生任何明显现象你认为没有产生明显现象的原因是(1)氢氧化钠溶液与稀盐酸反应生成氯化钠和水,反应无明显现象
【2】教材中将少量酚酞试液滴加到氢氧化钠溶液中,可观察到的现象是(2)溶液由无色变为红色
再逐滴向此烧杯中加入稀盐酸并不断搅拌当观察到(3)溶液由红色变为无色现象则说明溶液中的氢氧化钠已完全反应,因此他们得出如下结论若要证明两种物质能发生化学反应,一般可以考虑两个方面.一:看是否有新物质生成;二:(4)看反应物是否被消耗.
分析 【1】根据氢氧化钠溶液与稀盐酸反应生成氯化钠和水,进行分析解答.
【2】酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色,结合氢氧化钠溶液与稀盐酸发生中和反应生成氯化钠和水,进行分析解答.
解答 解:【1】氢氧化钠溶液与稀盐酸反应生成氯化钠和水,反应无明显变化,故没有产生任何明显现象.
【2】酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色,教材中将少量酚酞试液滴加到氢氧化钠溶液中,溶液由无色变为红色;再逐滴向此烧杯中加入稀盐酸并不断搅拌,氢氧化钠溶液与稀盐酸发生中和反应生成氯化钠和水,当恰好完全反应时,生成的氯化钠溶液显中性,当观察到溶液由红色变为无色,则说明溶液中的氢氧化钠已完全反应.
若要证明两种物质能发生化学反应,一般可以考虑两个方面.一:看是否有新物质生成;二:可以看反应物是否被消耗.
故答案为:【1】氢氧化钠溶液与稀盐酸反应生成氯化钠和水,反应无明显现象.
【2】溶液由无色变为红色;溶液由红色变为无色;看反应物是否被消耗.
点评 本题难度不大,掌握中和反应的原理、常见酸碱指示剂的性质是正确解答本题的关键.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
14.元素X的原子结构示意图为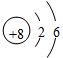 ,下列说法不正确的是( )
,下列说法不正确的是( )
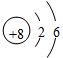 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | X的常见单质的化学式可表示为X2 | |
| B. | X的常见单质具有可燃性 | |
| C. | 酒精在X的常见单质中燃烧生成CX2和H2X | |
| D. | 在人体组织里,葡萄糖在酶的催化作用下跟X的常见单质反应产生共机体活动和维持恒定体温的能量 |
15.重铬酸钾(K2Cr2O7)酸性水溶液可以检测乙醇,遇到乙醇会迅速变成灰绿色,可应用于酒驾检查,在重铬酸钾中铬元素(Cr)的化合价是( )
| A. | +4价 | B. | +5价 | C. | +6价 | D. | +7价 |
19.氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La),其中子数为57的说法不正确的是( )
| A. | 该元素原子的质子数为57 | B. | 该元素原子的核电荷数为57 | ||
| C. | 该元素原子的相对原子质量为114 | D. | 该元素为非金属元素 |
9.下列物质敞口放置在空气中质量会增加的是( )
①浓硫酸 ②浓盐酸 ③纯碱 ④烧碱 ⑤生石灰.
①浓硫酸 ②浓盐酸 ③纯碱 ④烧碱 ⑤生石灰.
| A. | ①②③④⑤ | B. | ①③④⑤ | C. | ①④⑤ | D. | ①④ |
16. 如图是汽车“尾气催化转换器”中将尾气中有毒气体转变为无毒气体的微观示意图.下列说法正确的是( )
如图是汽车“尾气催化转换器”中将尾气中有毒气体转变为无毒气体的微观示意图.下列说法正确的是( )
 如图是汽车“尾气催化转换器”中将尾气中有毒气体转变为无毒气体的微观示意图.下列说法正确的是( )
如图是汽车“尾气催化转换器”中将尾气中有毒气体转变为无毒气体的微观示意图.下列说法正确的是( )| A. | 分子在化学变化中可以再分 | |
| B. | 原子在化学变化中是不可再分的 | |
| C. | 图中所示反应中,反应物的分子个数比为3:2 | |
| D. | 该反应中有两种物质生成 |
14.小明同学对所学部分化学知识归纳如下,其中有错误的一组是( )
| A | 初中化学中常见的“最” | B | 物质与粒子的关系 |
| 天然存在的最硬的物质是金刚石 相同条件下密度最小的气体 H2 地壳中含量最多的元素是---O | 金属汞是由分子构成 氧气是由原子构成 氯化钠是由离子构成 | ||
| C | 元素符号周围数字的含义 | D | 元素的知识 |
| 正上方数字表示元素的化合价 前面的数字表示原子的个数 右下方数字表示一个分子中含有的原子数 | 决定元素的种类是质子数 决定元素化学性质---是原子的最外层电子数 决定元素在元素周期表中排列顺序是质子数 |
| A. | A | B. | B | C. | C | D. | D |
 下列A--D是初中科学常见物质,其中A为含三种元素的钠盐,C为大理石的主要成分,B是两种元素组成的纯净物,它们之间存在如图所示的关系(连线表示会发生化学反应,箭头表示通过反应可以生成某物质):
下列A--D是初中科学常见物质,其中A为含三种元素的钠盐,C为大理石的主要成分,B是两种元素组成的纯净物,它们之间存在如图所示的关系(连线表示会发生化学反应,箭头表示通过反应可以生成某物质):