��Ŀ����
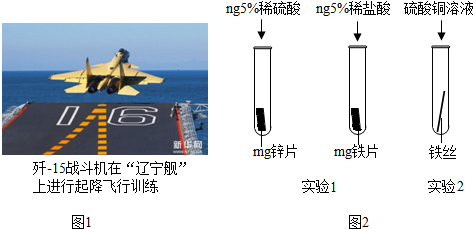
���������ڹ���������������Ҫ�����ã�ͼ1Ϊ��-15�ɻ��ں���ĸ������ɣ�
��1�����������д���ʹ�õ��ǺϽ�����Ǵ�������������Ϊ�Ͻ���и����������ܣ��������Ͻ�ȴ�����Ӳ�� �����С������
��2���ճ�����������Ʒ��������ʴ��ԭ���� ���û�ѧ����ʽ��ʾ����
��3����������ʴ��Ҫ����������е� �� ��ͬ���õĽ����
��4��Ϊ�˱����ִ��ĸ�����DZ���ʴ��ͨ�����ִ��������Ƕ�������ǿ������С��Ϊ̽��п������ͭ���ֽ����Ļ��˳���������ͼ2������ʵ�飺
��ʵ��1�У�С���ԡ���������������ݵĿ�����Ϊ�����ж�п�����Ļ��ǿ������ͬѧ��Ϊ���������������� ��
��ʵ��2������ ����֤�����Ļ��ǿ��ͭ��
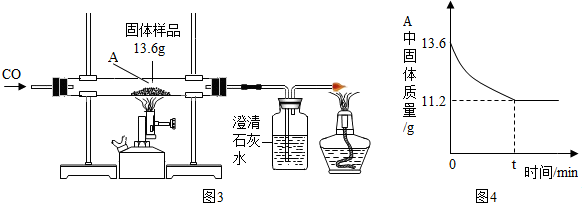
��5��ij��ȤС���һ�ݺ����Ĺ�����Ʒ����̽����ͨ��ʵ����ȷ������Ʒ�������������ۻ�϶��ɣ����dz�ȡ��13.6g������Ʒ����ͼ3��ʾ��װ��ʵ�飬�ⶨ��������ͼ4��ʾ��
��ͼ3��Ӳ�ʲ������е��������Ļ�ѧ����ʽΪ ��
�ڹ�����Ʒ���������������� �ˣ�
�۽�������Ӧ��11.2g�Ĺ����м���100gϡ���ᣬǡ����ȫ��Ӧ����Ӧ��������Һ�����ʵ��������� �������ȷ��0.1%������д������̣���

��1�����������д���ʹ�õ��ǺϽ�����Ǵ�������������Ϊ�Ͻ���и����������ܣ��������Ͻ�ȴ�����Ӳ��
��2���ճ�����������Ʒ��������ʴ��ԭ����
��3����������ʴ��Ҫ����������е�
��4��Ϊ�˱����ִ��ĸ�����DZ���ʴ��ͨ�����ִ��������Ƕ�������ǿ������С��Ϊ̽��п������ͭ���ֽ����Ļ��˳���������ͼ2������ʵ�飺
��ʵ��1�У�С���ԡ���������������ݵĿ�����Ϊ�����ж�п�����Ļ��ǿ������ͬѧ��Ϊ����������������
��ʵ��2������
��5��ij��ȤС���һ�ݺ����Ĺ�����Ʒ����̽����ͨ��ʵ����ȷ������Ʒ�������������ۻ�϶��ɣ����dz�ȡ��13.6g������Ʒ����ͼ3��ʾ��װ��ʵ�飬�ⶨ��������ͼ4��ʾ��
��ͼ3��Ӳ�ʲ������е��������Ļ�ѧ����ʽΪ
�ڹ�����Ʒ����������������
�۽�������Ӧ��11.2g�Ĺ����м���100gϡ���ᣬǡ����ȫ��Ӧ����Ӧ��������Һ�����ʵ���������

���㣺�Ͻ���Ͻ������,������Ե�̽��,�й��������������ļ���,�����Ļ�ѧ����,һ����̼��ԭ������,������ʴ�������������,���ݻ�ѧ��Ӧ����ʽ�ļ���
ר�⣺�������������
��������1���ӺϽ������һ��ȴ������Ĵ�ȥ������
��2�������Ϳ����е�������Ӧ����һ�����ܵ���������Ĥ����ֹ�����������ĽӴ�����ֹ�����Ľ�һ����ʴȥ������
��3���Ӹ�������ʴ��Ҫ����������е�������ˮ�������ӵĻ�ѧ��Ӧȥ������
��4����������ѡȡ��������ͬ�����Բ�������
�ڰ����ŵ�����ͭ��Һ�У������˿������ֺ�ɫ���ʣ�˵�������û�������ͭ�е�ͭ��
��5����������ԭ�����ڸ������������û�ԭ��һ����̼�����������������л�ԭ������
����ͼ�п��Կ��������й��������������������Ԫ�ص����������ݷ������
�����ڷ�Ӧ�����õ���Һ�е��������Ȼ����������ݻ�ѧ����ʽ���м��㣮
��2�������Ϳ����е�������Ӧ����һ�����ܵ���������Ĥ����ֹ�����������ĽӴ�����ֹ�����Ľ�һ����ʴȥ������
��3���Ӹ�������ʴ��Ҫ����������е�������ˮ�������ӵĻ�ѧ��Ӧȥ������
��4����������ѡȡ��������ͬ�����Բ�������
�ڰ����ŵ�����ͭ��Һ�У������˿������ֺ�ɫ���ʣ�˵�������û�������ͭ�е�ͭ��
��5����������ԭ�����ڸ������������û�ԭ��һ����̼�����������������л�ԭ������
����ͼ�п��Կ��������й��������������������Ԫ�ص����������ݷ������
�����ڷ�Ӧ�����õ���Һ�е��������Ȼ����������ݻ�ѧ����ʽ���м��㣮
����⣺��1���Ͻ������һ��ȴ������Ĵ��������Ͻ��Ӳ�ȱȴ����ʴ�Ϊ����
��2���������Ϳ����е�������Ӧ����һ�����ܵ���������Ĥ����ֹ�����������ĽӴ�����ֹ�����Ľ�һ����ʴ���ʴ�Ϊ��4Al+3O2�T2Al2O3
��3����������ʴ��Ҫ����������е�������ˮ�������ӵĻ�ѧ��Ӧ���ʴ�Ϊ������ ˮ��
��4����������ѡȡ��������ͬ�����Բ��������ʴ�Ϊ����ȡ������ͬ��
�ڰ����ŵ�����ͭ��Һ�У������˿������ֺ�ɫ���ʣ�˵�������û�������ͭ�е�ͭ��˵�����Ļ�Ա�ͭǿ���ʴ�Ϊ����˿������ֺ�ɫ���ʣ�
��5����������ԭ�����ڸ������������û�ԭ��һ����̼�����������������л�ԭ�������䷴Ӧ�Ļ�ѧ����ʽΪ��Fe2O3+3CO
2Fe+3CO2���ʴ�Ϊ��Fe2O3+3CO
2Fe+3CO2��
�ڽ⣺��������������Ϊx����
3CO+Fe2O
2Fe+3CO2 �������
160 ��112 160-112=48
x ��13.6g-11.2 g��
=
���x=8g
�ʴ�Ϊ��8��
�������ɵ�FeCl2��H2�����ֱ�Ϊx��y����
Fe+2HCl=FeCl2+H2��
56 127 2
11.2g x y
=
=
���x=25.4g��y=0.4g
���ڷ�Ӧ�����õ���Һ�е��������Ȼ����������Ȼ���������������Ϊ
��
��100%=22.9%��
�ʴ�Ϊ��22.9%
��2���������Ϳ����е�������Ӧ����һ�����ܵ���������Ĥ����ֹ�����������ĽӴ�����ֹ�����Ľ�һ����ʴ���ʴ�Ϊ��4Al+3O2�T2Al2O3
��3����������ʴ��Ҫ����������е�������ˮ�������ӵĻ�ѧ��Ӧ���ʴ�Ϊ������ ˮ��
��4����������ѡȡ��������ͬ�����Բ��������ʴ�Ϊ����ȡ������ͬ��
�ڰ����ŵ�����ͭ��Һ�У������˿������ֺ�ɫ���ʣ�˵�������û�������ͭ�е�ͭ��˵�����Ļ�Ա�ͭǿ���ʴ�Ϊ����˿������ֺ�ɫ���ʣ�
��5����������ԭ�����ڸ������������û�ԭ��һ����̼�����������������л�ԭ�������䷴Ӧ�Ļ�ѧ����ʽΪ��Fe2O3+3CO
| ||
| ||
�ڽ⣺��������������Ϊx����
3CO+Fe2O
| ||
160 ��112 160-112=48
x ��13.6g-11.2 g��
| 160 |
| 48 |
| x |
| (13.6g-11.2g) |
���x=8g
�ʴ�Ϊ��8��
�������ɵ�FeCl2��H2�����ֱ�Ϊx��y����
Fe+2HCl=FeCl2+H2��
56 127 2
11.2g x y
| 56 |
| 127 |
| 11.2g |
| x |
| 56 |
| 2 |
| 11.2g |
| y |
���x=25.4g��y=0.4g
���ڷ�Ӧ�����õ���Һ�е��������Ȼ����������Ȼ���������������Ϊ
��
| 25.4g |
| 11.2g+100g-0.4g |
�ʴ�Ϊ��22.9%
�����������ۺ��Խ�ǿ���ر����йػ�ѧ����ʽ�ļ��㣬��Ҫͬѧ���ܹ�ȷ����д��ѧ����ʽ���������ʼ�Ĺ�ϵ���ſ�����ȷ�ļ��㣮

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
�������ʵ���;�У�ֻ�����仯ѧ���ʵ��ǣ�������
| A�����ʯ������̽��Ӳ���Ҳ� |
| B��������̼������� |
| C�������������� |
| D��ʯī������ |
̼�ĵ����У��ʵؽ������������缫���ǣ�������
| A�����ʯ |
| B������̿ |
| C��C60 |
| D��ʯī |
�����йؽ������������ϵ�˵������ȷ���ǣ�������
| A������������Ԫ������Ȼ�����Ե�����ʽ���� |
| B��Ӳ������ͭ�ֶ��ǺϽ� |
| C������Ŀǰ�����������ߵĽ��� |
| D����ʴ��Ľ�����Ʒû�л������õļ�ֵ |
 ��������M��N���ֽ�������֪M��N���������о�Ϊ+2�ۣ����ֱ�����ͬ������������ͬ������ϡ���ᷴӦ���������������ͷ�Ӧʱ��Ĺ�ϵ��ͼ��ʾ������������ȷ���ǣ�������
��������M��N���ֽ�������֪M��N���������о�Ϊ+2�ۣ����ֱ�����ͬ������������ͬ������ϡ���ᷴӦ���������������ͷ�Ӧʱ��Ĺ�ϵ��ͼ��ʾ������������ȷ���ǣ�������| A��M��N���ֽ����нϻ��õ���N |
| B������H2������M��N |
| C��M��N�����ԭ������һ����M��N |
| D����Ӧ��ȫ�����������ģ�������Ӧ�� |


 CO��һ����ɫ����ζ���ж��Ŀ�ȼ������Ⱦ����л�ԭ�ԣ�������ұ��ҵ��ij��ȤС��Ϊ̽������л�ԭ�ԣ����������ʵ��װ�ã���ش������й����⣺
CO��һ����ɫ����ζ���ж��Ŀ�ȼ������Ⱦ����л�ԭ�ԣ�������ұ��ҵ��ij��ȤС��Ϊ̽������л�ԭ�ԣ����������ʵ��װ�ã���ش������й����⣺