题目内容
10. A~J都是初中化学中的常见物质,且有如图所示转化关系(反应条件其他生成物均已略去).已知A为金属单质、其它均为化合物,C为大理石的主要成分,E为一种常见的不挥发性酸,I物质中含钠元素,回答下列问题:
A~J都是初中化学中的常见物质,且有如图所示转化关系(反应条件其他生成物均已略去).已知A为金属单质、其它均为化合物,C为大理石的主要成分,E为一种常见的不挥发性酸,I物质中含钠元素,回答下列问题:(1)写出下列物质的化学式:ACu、FCa(OH)2,JCu(OH)2
(2)写出下列反应方程式:J+E:H2SO4+Cu(OH)2═CuSO4+2H2O,G+H:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
分析 根据题干提供额信息进行分析解答,A是金属单质,能最终转化生成蓝色沉淀,故A可能是铜,生成的B是氧化铜,E是一种常见的不挥发性酸,氧化铜能与E酸反应生成D,故E是硫酸,D是硫酸铜;C为大理石的主要成分,故C是碳酸钙,碳酸钙能高温分解生成氧化钙和二氧化碳,F能与水反应生成G,故F可能是氧化钙,G是氢氧化钙,氢氧化钙能与碳酸钠反应生成氢氧化钠,氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀,故H是碳酸钠,I是氢氧化钠,据此解答.
解答 解:A是金属单质,能最终转化生成蓝色沉淀,故A可能是铜,生成的B是氧化铜,E是一种常见的不挥发性酸,氧化铜能与E酸反应生成D,故E是硫酸,D是硫酸铜;C为大理石的主要成分,故C是碳酸钙,碳酸钙能高温分解生成氧化钙和二氧化碳,F能与水反应生成G,故F可能是氧化钙,G是氢氧化钙,氢氧化钙能与碳酸钠反应生成氢氧化钠,氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀,故H是碳酸钠,I是氢氧化钠,带入框图,推断合理;
(1)A是铜,F是氢氧化钙,J是氢氧化铜,故填:Cu,Ca(OH)2,Cu(OH)2;
(2)氢氧化铜能与硫酸反应生成硫酸铜和水,故填:H2SO4+Cu(OH)2═CuSO4+2H2O;
氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故填:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 本题为框图式物质推断题,解答本题的关键是根据解题突破口直接得出有关物质的化学式,然后推断得出其他物质的化学式,书写反应的化学方程式要注意配平.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.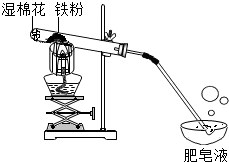 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如图所示实验,探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如图所示实验,探究铁粉与水蒸气反应后的产物.
(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.该黑色固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.铁和水蒸气反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】已知:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,完成下列实验探究:
 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如图所示实验,探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如图所示实验,探究铁粉与水蒸气反应后的产物.(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】已知:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,完成下列实验探究:
| 实验操作 | 实验现象 | 结论 |
| 猜想一成立 | ||
| 猜想二成立 |
1.环境和能源是人类生存和发展的基本条件.下列有关环境和能源的说法错误的是( )
| A. | 二氧化碳是造成温室效应的主要物质 | |
| B. | 塑料袋给我们生活带来了很大便利,应大力提倡使用 | |
| C. | 太阳能、潮汐能、风能是人类正在开发和利用的重要能源 | |
| D. | 煤、石油、天然气是三种重要的化石燃料,不完全燃烧会造成空气污染 |
2.除去下列物质中混有少量杂质(括号内为杂质),所用除杂试剂及操作方法均正确的是( )
| 选项 | 物质 | 试剂 | 操作方法 |
| A | CO2(CO) | O2 | 点燃 |
| B | FeSO4(H2SO4) | 加入过量的氧化铁 | 充分反应后过滤 |
| C | CaO(CaCO3) | 稀盐酸 | 滴加适量稀盐酸 |
| D | Cu(Fe) | 稀硫酸 | 先加入适量稀硫酸,再过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |