题目内容
5.青少年摄入锌不足会引起食欲不振,生长迟缓,发育不良,缺锌者可在医生指导下服用葡萄糖酸锌口服液来补锌.已知葡萄糖酸锌的化学式为C12H22O14Zn,其相对分子质量为455.下列说法正确的是( )| A. | 葡萄糖酸锌中锌元素的质量分数为31.6% | |
| B. | 葡萄糖酸锌不是氧化物 | |
| C. | 葡萄糖酸锌中碳、氢元素质量比为6:11 | |
| D. | 葡萄糖酸锌是由12个碳原子、22个氢原子、14个氧原子和1个锌原子构成的 |
分析 A.根据化合物中元素的质量分数计算方法来分析;
B.氧化物是只含有两种元素且其中一种元素是氧元素的化合物;
C.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断;
D.根据葡萄糖酸锌的微观构成进行分析判断.
解答 解:A.葡萄糖酸锌中锌元素的质量分数为$\frac{65}{12×12+1×22+16×14+65}$×100%≈14.3%,故错误;
B.葡萄糖酸锌是由碳、氢、氧、锌四种元素组成的纯净物,不属于氧化物,故正确;
C.葡萄糖酸锌中碳、氢元素质量比为(12×12):(1×22)≠6:11,故错误;
D.葡萄糖酸锌是由葡萄糖酸锌分子构成的,1个葡萄糖酸锌分子是由12个碳原子、22个氢原子、14个氧原子和1个锌原子构成的,故错误.
故选:B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列实验操作不能达到目的是( )
| A. | 海水淡化:蒸馏 | |
| B. | 除去粗盐中的不溶物:溶解、过滤、蒸发 | |
| C. | 鉴别H2和CO:点燃,观察火焰 | |
| D. | 除去Cu粉中的Fe:加入稀盐酸,过滤 |
13.(1)在下表的空白处填上恰当的内容:
(2)小丽同学做完镁条在空气中燃烧的实验之后,对该变化的实质进行研究,氧原子和镁原子的结构示意图如图1所示,从氧原子和镁原子的结构示意图可以看出,氧原子和镁原子结合时,氧原子易得到2个电子,镁原子易失去2个电子,形成的两种粒子的符号分别是O2-、Mg2+.
②镁条在空气中燃烧的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(3)如图2是两种物质发生中和反应的微观示意图,请回答下列问题:
①图中发生中和反应的化学方程式为:HCl+NaOH=NaCl+H2O.
②当恰好完全中和后,反应的实质可以用一个式子表示为H++OH-=H2O,此时溶液中存在的离子是Na+、Cl-(填符号).

| 物质名称 | 物质的组成(用化学式表示) | 构成物质的微粒(用符号表示) |
| 干冰 | ||
| 锌 | ||
| 食盐水 | ---------- |
②镁条在空气中燃烧的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(3)如图2是两种物质发生中和反应的微观示意图,请回答下列问题:
①图中发生中和反应的化学方程式为:HCl+NaOH=NaCl+H2O.
②当恰好完全中和后,反应的实质可以用一个式子表示为H++OH-=H2O,此时溶液中存在的离子是Na+、Cl-(填符号).

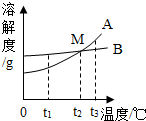 右图是A、B的溶解度曲线.
右图是A、B的溶解度曲线.