题目内容
1.同学们在实验室进行如图所示两个实验,图1是加热使水沸腾实验,图2是电解水实验,
a管内气体是氢气,a管和b管中气体体积比为2:1.
如何检验b管气体:将带火星的木条放在试管口,若木条复燃,说明是氧气.
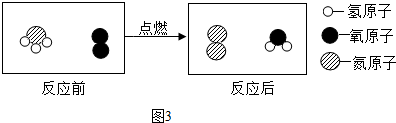
从微观角度解释这两个实验的本质不同图1实验没有新物质生成,分子本身没有发生改变,只是温度升高,水分子之间的间隙变大;图2实验水分子分裂成了氢原子和氧原子,然后氢原子、氧原子分别重新组合形成氢分子、氧分子.
分析 根据电解水的实验现象、结论:电解水时,与电源正极相连的试管内产生的气体体积少,能使带火星的木条复燃,是氧气;与电源负极相连的试管内的气体体积多,能燃烧,是氢气;且两者的体积之比大约是1:2;进行分析解答即可.
加热使水沸腾,没有新物质生成,属于物理变化;电解水生成氢气和氧气,有新物质生成,属于化学变化;据此进行分析解答.
解答 解:在电解水的实验中,所用的电源是直流电;与电源正极相连的试管内产生的气体体积少,能使带火星的木条复燃,是氧气;另一只试管内的气体能燃烧,是氢气;则a管与电源的负极相连,管内气体是氢气,a管和b管中气体体积比为两种气体的体积比为2:1.
b管气体是氧气,氧气能支持燃烧,检验方法是将带火星的木条放在试管口,若木条复燃,说明是氧气.
图1的实验是物理变化,没有新物质生成,分子本身没有发生改变,只是温度升高,水分子之间的间隙变大;图2是水通过电解生成了新物质氢气和氧气,水分子分裂成了氢原子和氧原子,然后氢原子、氧原子分别重新组合形成氢分子、氧分子,大量的氢分子、氧分子分别聚集成氢气、氧气,该事实说明分子是可以再分的.
故答案为:氢气;2:1;将带火星的木条放在试管口,若木条复燃,说明是氧气;图1实验没有新物质生成,分子本身没有发生改变,只是温度升高,水分子之间的间隙变大;图2实验水分子分裂成了氢原子和氧原子,然后氢原子、氧原子分别重新组合形成氢分子、氧分子.
点评 本题难度不大,掌握电解水的实验现象、结论(正氧负氢、氢二氧一)等是正确解答本题的关键.

练习册系列答案
相关题目
16.逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
| A. | 因为H2O和H2O2组成元素相同,所以它们的化学性质相同 | |
| B. | 因为pH>7的溶液显碱性,所以pH>7的溶液都是碱溶液 | |
| C. | 因为有机物中都含有碳元素,所以含碳元素的物质都是有机物 | |
| D. | 因为化学反应前后原子种类不变,所以化学反应前后元素种类也不变 |
17.根据下列原子结构示意图判断,化学性质相似的是( )


| A. | ①② | B. | ②④ | C. | ②③ | D. | ①④ |
14.下列食物中富含维生素C的是( )
| A. | 肥西老母鸡 | B. | 大圩葡萄 | C. | 下塘烧饼 | D. | 磨店老豆腐 |
1. 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据图的溶解度曲线
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据图的溶解度曲线
判断下列说法,其中正确的是( )
 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据图的溶解度曲线
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据图的溶解度曲线判断下列说法,其中正确的是( )
| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | 40℃时,两种物质溶液的质量分数相同 | |
| C. | 60℃时,将60g乙物质放入100g水中,所得溶液的质量为160g | |
| D. | 甲中混有少量的乙,可以采用降温结晶的方法提纯甲 |
10.关于金属的性质,下列化学方程式的表示符合题意,且书写正确的是( )
| A. | 铁在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 铝在空气中形成致密的氧化膜:4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3 | |
| C. | 鉴别黄铜和黄金:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO | |
| D. | 镁在氧气中燃烧:Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 |