题目内容
9.将少量白砂糖加热,白糖会慢慢融化为液体,这时白糖发生了物理变化;若继续加热,白糖会逐渐变黑,并闻到有一股焦糊味,这时白糖发生的变化属于化学变化,理由是有新物质生成.分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
解答 解:将少量白砂糖加热,白糖会慢慢融化为液体,此过程中只是状态发生改变,没有新物质生成,属于物理变化;若继续加热,白糖会逐渐变黑,并闻到有一股焦糊味,此过程中有新物质生成,属于化学变化.
故填:物理;化学;有新物质生成.
点评 本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
20.下列有关溶液的说法中正确的是( )
| A. | 均一、稳定的液体都是溶液 | |
| B. | 饱和溶液一定比不饱和溶液浓 | |
| C. | 溶液一定是液体 | |
| D. | 餐具上的油污可利用洗涤剂的乳化功能将其洗去 |
17.小兴趣小组同学发现实验台上整齐摆放的药品中(见图),有一试剂瓶的标签破损.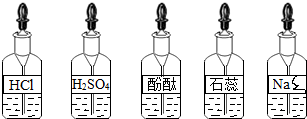
【提出问题】这瓶试剂的成分是什么?
【讨论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是酸(填物质类别);
【猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaHCO3溶液.
【设计并实验】
(1)小明用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断这是一种碱性溶液.对他的操作方法、测量结果及结论的评价,正确的是B;
A.方法正确,结果正确,且结论正确
B.方法不正确,结果偏小,但结论正确
C.方法不正确,结果偏大,结论不正确
D.方法正确,结果正确,但结论不正确
(2)小明认为它是NaOH溶液,小俊认为它是Na2CO3溶液.要进一步确定它的成分,小俊认为只需选择上图已有的试剂就能把它鉴别出来.他们又进行了实验.
(3)小丽同学在做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生.怀疑是不是拿错了药品?经检验确认没有拿错药品,而是氢氧化钠溶液变质了.
【进一步实验】小丽同学要用此溶液制取纯净的氢氧化钠溶液,继续完成中和反应实验.请你帮助她解决该问题:
取该氢氧化钠溶液于试管中,加入适量的氢氧化钙溶液,至溶液中不再产生沉淀为止,过滤,得到溶液即可继续使用.

【提出问题】这瓶试剂的成分是什么?
【讨论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是酸(填物质类别);
【猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaHCO3溶液.
【设计并实验】
(1)小明用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断这是一种碱性溶液.对他的操作方法、测量结果及结论的评价,正确的是B;
A.方法正确,结果正确,且结论正确
B.方法不正确,结果偏小,但结论正确
C.方法不正确,结果偏大,结论不正确
D.方法正确,结果正确,但结论不正确
(2)小明认为它是NaOH溶液,小俊认为它是Na2CO3溶液.要进一步确定它的成分,小俊认为只需选择上图已有的试剂就能把它鉴别出来.他们又进行了实验.
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取少量样品于试管中 向其中滴入适量的稀盐酸 | 有气泡产生 | 猜想②正确 相关的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
【进一步实验】小丽同学要用此溶液制取纯净的氢氧化钠溶液,继续完成中和反应实验.请你帮助她解决该问题:
取该氢氧化钠溶液于试管中,加入适量的氢氧化钙溶液,至溶液中不再产生沉淀为止,过滤,得到溶液即可继续使用.
4.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动,以下是教学片断,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式:H2SO4+2NaOH=Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下,请你补上猜想四.
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH 猜想四:有Na2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想三,理由是H2SO4和NaOH在溶液中不能共存.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用了老师提供的pH试纸、Na2CO3溶液、BaCl2溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予了肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了如下两处错误:
①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中也有一个是错误的,错误的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式:H2SO4+2NaOH=Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下,请你补上猜想四.
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH 猜想四:有Na2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想三,理由是H2SO4和NaOH在溶液中不能共存.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用了老师提供的pH试纸、Na2CO3溶液、BaCl2溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液的pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  | 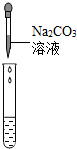 | 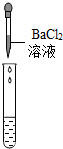 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予了肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了如下两处错误:
①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中也有一个是错误的,错误的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
1. 酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这两类化合物进行了一系列的探究活动.
酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这两类化合物进行了一系列的探究活动.
(1)同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是为什么?
(2)如图是某试剂瓶标签上的内容.要把10 g这种浓硫酸稀释为20%的硫酸,需要水的质量为39g.
稀释浓硫酸时,不可将水倒进浓硫酸里,请解释其原因.
(3)氢氧化钠暴露在空气中会变质,写出氢氧化钠变质的化学方程式:2NaOH+CO2═Na2CO3+H2O.
①取少量该固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,说明该样品中含有碳酸钠,由此可确定该固体已发生变质.则无色溶液可能是盐酸.
②为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如表所示的实验.已知碳酸钠的水溶液呈碱性,它的存在会对氢氧化钠的检验造成干扰.请根据如图部分物质的溶解性表(20℃)所提供的信息,将如表填写完整.
(4)若73 g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数.
 酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这两类化合物进行了一系列的探究活动.
酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这两类化合物进行了一系列的探究活动.(1)同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是为什么?
(2)如图是某试剂瓶标签上的内容.要把10 g这种浓硫酸稀释为20%的硫酸,需要水的质量为39g.
稀释浓硫酸时,不可将水倒进浓硫酸里,请解释其原因.
(3)氢氧化钠暴露在空气中会变质,写出氢氧化钠变质的化学方程式:2NaOH+CO2═Na2CO3+H2O.
①取少量该固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,说明该样品中含有碳酸钠,由此可确定该固体已发生变质.则无色溶液可能是盐酸.
②为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如表所示的实验.已知碳酸钠的水溶液呈碱性,它的存在会对氢氧化钠的检验造成干扰.请根据如图部分物质的溶解性表(20℃)所提供的信息,将如表填写完整.
| 阳离子 | OH | N03- | C1- | SO42- | C03- |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不溶 | 不溶 |
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的氯化钡溶液 充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为 Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 检验是否含有氢氧化钠 | 在滤液中滴加酚酞溶液 | 溶液变红色 | 该样品中含有氢氧化钠 |
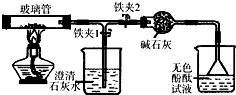
 根据如图所示的信息,回答下列问题.
根据如图所示的信息,回答下列问题.