题目内容
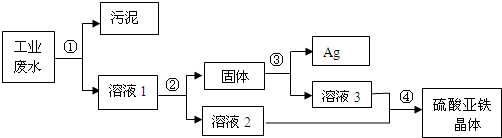
有一种工业废水,其中含有大量的硫酸亚铁,少量的银离子以及污泥。某同学设计了一个既经济又合理的方法回收银和硫酸亚铁晶体。方案流程如下: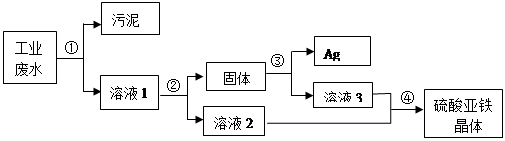
回答下列问题:
(1)步骤②中:需加入的物质是 ,分离所得混合物的方法是 。
(2)步骤③中:需加入的物质是 ,发生反应的化学方程式是 。
(3)某同学认为经过步骤②后所得固体就是纯净的银,不需要进行步骤③,你认为是否合理? ,理由是 。
(4)步骤④的操作是 ,溶液2和溶液3为什么要混合? 。
(1). Fe 过滤 (2)稀硫酸 Fe+H2SO4=FeSO4+H2 ↑
(3) 不合理 因为要使Ag+ 完全置换出来,必须加入过量的铁
(4) 降温结晶 两种滤液中都含有硫酸亚铁,可得到更多的硫酸亚铁,综合利用
解析试题分析:(1) 步骤②中:需加入的物质是铁,置换出银,同时不引入新的杂质,可以用过滤的方式分离所得混合物;(2)步骤③中:需加入的物质是稀硫酸,目的是除去过量的铁,发生的反应是铁和稀硫酸生成硫酸亚铁和氢气;(3)不合理,固体混合物中含有过量的铁,必须经过步骤③除掉;(4)通过降温结晶的方法可以得到硫酸亚铁晶体,溶液2和溶液3混合是为了得到更多的硫酸亚铁,综合利用,因为两种滤液中都含有硫酸亚铁。
考点:工业废水的处理
点评:中考中常在选择题和填空题中考察化学反应流程图类型的题目,每年必有,同学们应注意在平时的学习中多多积累总结。

练习册系列答案
相关题目