题目内容
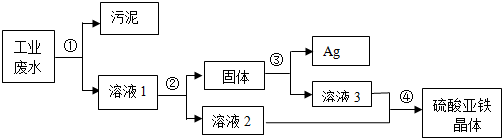
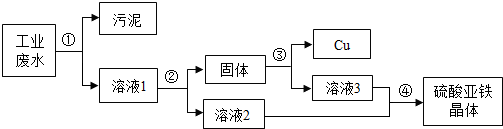
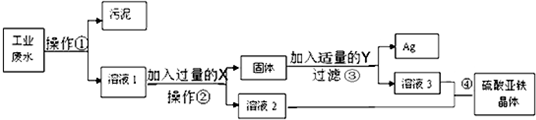
有一种工业废水,其中含有大量的硫酸亚铁、少量的银离子以及污泥.某同学设计了一个既经济又合理的方法回收银和硫酸亚铁晶体.方案流程如图所示:
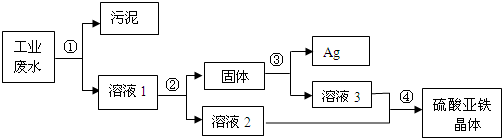
回答下列问题:
A.步骤②中:需加入的物质是 .
B.步骤③中发生反应的化学方程式是 .

回答下列问题:
A.步骤②中:需加入的物质是
B.步骤③中发生反应的化学方程式是
分析:(1)此过程是对银的分离,为了不引入新的杂质此处应放金属铁,由于是溶液与银的分离故可采用过滤的方法完成;
(2)由于固体中含有银与过量的铁,所以要得到纯净的银应该消耗掉金属铁,加稀硫酸可使铁被消耗,再根据化学方程式书写注意事项考虑.
(2)由于固体中含有银与过量的铁,所以要得到纯净的银应该消耗掉金属铁,加稀硫酸可使铁被消耗,再根据化学方程式书写注意事项考虑.
解答:解:(1)此过程是置换出银的过程,为了在不引入新的杂质的前提下用金属铁置换较为合适;
(2)为把银能彻底置换出来加入铁的质量应该是过量的,因此固体中含有银与过量的铁,所以要得到纯净的银应该消耗掉金属铁,加稀硫酸可使铁被消耗又不引入新的杂质,所以③方程式是铁与硫酸反应生成硫酸亚铁和氢气,所以方程式是:Fe+H2SO4═FeSO4+H2↑.
故答案为:铁;Fe+H2SO4═FeSO4+H2↑.
(2)为把银能彻底置换出来加入铁的质量应该是过量的,因此固体中含有银与过量的铁,所以要得到纯净的银应该消耗掉金属铁,加稀硫酸可使铁被消耗又不引入新的杂质,所以③方程式是铁与硫酸反应生成硫酸亚铁和氢气,所以方程式是:Fe+H2SO4═FeSO4+H2↑.
故答案为:铁;Fe+H2SO4═FeSO4+H2↑.
点评:此题是一道金属回收题,解题的关键是要明确回收的原理,结合题目内的框题进行分析探讨,是一道分离混合物的综合题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目