题目内容
4.在食盐中加入碘酸钾(KIO3)可以预防碘缺乏病.测定市场销售的食盐中是否含有碘元素的方法是:将食盐在酸性条件下与碘化钾溶液(KI)反应生成碘单质(I2),碘单质遇淀粉变蓝.反应的化学方程式为:KIO3+5KI+6HCl═6KCl+3I2+3H2O,现有1千克市售食盐,为测定含碘酸钾的量,取其中的20克食盐,完全反应用掉0.01%碘化钾溶液41.5克,求这1千克食盐中碘元素质量?分析 由于给出了消耗的0.01%碘化钾溶液41.5克,所以可以根据化学方程式找出碘元素和碘化钾的质量对应关系,求算出20g食盐中含有的碘元素,进而求算1千克食盐中碘元素的质量.
解答 解:设20g食盐中含有的碘元素的质量为x
0.01%碘化钾溶液41.5克含有的碘化钾的质量为0.01%×41.5g=0.00415g
由KIO3+5KI+6HCl═6KCl+3I2+3H2O
可得食盐中碘元素与加入的碘化钾的关系为
I~~~5KI
127 830
x 0.00415g
$\frac{127}{830}$=$\frac{x}{0.00415g}$
x=0.000635g
则1千克食盐中碘元素的含量为0.000635g×$\frac{1000}{20}$=0.03175g
答:1千克食盐中碘元素的含量为0.03175g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
15.某花圃所种的花卉缺乏氮元素和钾元素,如果只施用一种化肥,则应施用( )
| A. | 硝酸钾 | B. | 碳酸钾 | C. | 尿素 | D. | 磷酸二氢钾 |
19.为达到实验目的,下表中实验材料选择不恰当的是( )
| 实验名称 | 实验材料 | 目的 | |
| A | 探究呼吸作用产生二氧化碳 | 氢氧化钠 | 检验是否产生二氧化碳 |
| B | 探究唾液对淀粉的消化作用 | 碘酒 | 检验淀粉是否被消化 |
| C | 绿叶在光下制造有机物 | 酒精 | 使叶绿素褪色 |
| D | 制作口腔上皮细胞临时装片 | 生理盐水 | 维持细胞正常形态 |
| A. | A | B. | B | C. | C | D. | D |
9.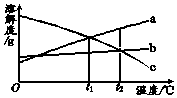 a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
 a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )| A. | 原饱和溶液中,溶质的质量分数a=c>b | |
| B. | 恢复至t1℃时,析出溶质的质量a=c>b | |
| C. | 恢复至t1℃时,三种溶液都是饱和溶液 | |
| D. | 若继续升温至t2℃,三种溶液都是饱和溶液 |
19.下列做法中不属于保护环境的是( )
| A. | 为了使农作物高产,施用大量的化肥 | |
| B. | 不乱砍乱伐,保护植物 | |
| C. | 将废旧垃圾统一回收处理 | |
| D. | 水龙头坏了及时修理 |
 2017年5月5日,中国首架无人机C919客机在浦东机场首飞成功.回答下列问题:
2017年5月5日,中国首架无人机C919客机在浦东机场首飞成功.回答下列问题:
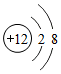 表示的是Mg2+(5)相对分子质量最小的单质是H2
表示的是Mg2+(5)相对分子质量最小的单质是H2