题目内容
14.取氢氧化铜和氢氧化镁组成的混合物7.8g,放入一定质量的溶质质量分数为10%的稀硫酸中,恰好完全反应,将所得溶液蒸发得到固体14g.则所用稀硫酸的质量是( )| A. | 50 g | B. | 100 g | C. | 49 g | D. | 98 g |
分析 最后得到的固体是有开始的氢氧化铜转化了硫酸铜,氢氧化镁转化为了硫酸镁,所以固体的质量变化可以求算参加反应的硫酸的质量,进而求算硫酸溶液的质量.
解答 解:设参加反应的硫酸的质量为x
由
Cu(OH)2+H2SO4=CuSO4+2H2O 固体质量变化量
98 98 160 160-98=62
Mg(OH)2+H2SO4=MgSO4+2H2O 固体质量变化量
58 98 120 62
可得关系式
H2SO4----------固体质量变化量
98 62
x 14g-7.8g=6.2g
$\frac{98}{62}$=$\frac{x}{6.2g}$
x=9.8g
则硫酸溶液的质量为$\frac{9.8g}{10%}$=98g
故选:D.
点评 本题在利用固体质量差量法的过程中发现了硫酸与固体质量变化之间的关系,也就是先利用了差量法后利用了关系式法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列物质在氧气中燃烧时,产生蓝紫色火焰的是( )
| A. | 木炭 | B. | 硫粉 | C. | 蜡烛 | D. | 红磷 |
2.氯化铵(NH4Cl)中氮元素的化合价是( )
| A. | +1 | B. | +3 | C. | +5 | D. | -3 |
9.下列实验中,水起隔绝氧气作用的是( )
| A. | 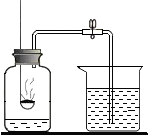 测空气中氧气含量 | B. | 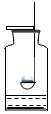 硫在氧气中燃烧 | ||
| C. |  燃烧条件的实验 | D. | 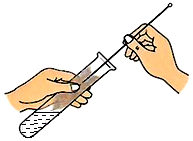 试管的洗涤 |
19.下列实验操作中,正确的是( )
| A. |  量取浓硫酸 | B. |  稀释浓硫酸 | ||
| C. |  装生锈铁钉 | D. |  倾倒稀硫酸 |
19.将m 克10%的NaOH溶液与m 克10%的硫酸溶液混合后,再滴入紫色石蕊试液,溶液显( )
| A. | 紫色 | B. | 红色 | C. | 蓝色 | D. | 无色 |

