题目内容
3.普通白炽灯和电暖气是家庭常用的照明取暖设备.依据下列问题试回答:
(1)上述图示中属于金属元素的是钨元素或铜元素或铝元素(或钨或铜或铝)(填元素名称,一种即可).
(2)物质的性质决定用途,用钨丝做灯丝是利用其熔点高的特点.金属铝应用十分广泛,有很强的抗腐蚀性,是因为常温下,铝的化学性质活泼,易被空气中的氧气氧化形成一层致密的氧化膜.
(3)铜和铝是常见的金属材料,试设计实验证明两者的活动性强弱2Al+3CuSO4=Al2(SO4)3+3Cu(用化学反应方程式表示).
分析 (1)金属材料包括金属单质和合金;非金属单质是指由非金属元素组成的单质;
(2)根据物质的性质,说出其用途;考虑铝易被空气中的氧气氧化形成一层致密的氧化膜;
(3)设计实验检验金属铝和铜活动性的强弱.
解答 解:(1)灯泡中铝、铜丝、钨丝都是金属单质,属于金属材料.
故答案为:钨或铜或铝;
(2)物质的性质决定用途,用钨丝做灯丝是利用其熔点高的特点.金属铝应用十分广泛,有很强的抗腐蚀性,是因为常温下,铝的化学性质活泼,易被空气中的氧气氧化形成一层致密的氧化膜.
(3)根据金属活动性,金属铝的活动性比铜强,所以,可以把铝放入可溶性铜盐溶液中,在铝表面得到红色金属铜,证明金属铝的活动性比铜强.则把铝片插入到CuSO4溶液中,其化学方程式为2Al+3CuSO4=Al2(SO4)3+3Cu.
故答案为:
(1)钨元素或铜元素或铝元素(或钨或铜或铝);
(2)熔点高;常温下,铝的化学性质活泼,易被空气中的氧气氧化形成一层致密的氧化膜;
(3)2Al+3CuSO4=Al2(SO4)3+3Cu(合理即可)
点评 本题考查了金属的物理性质和化学性质,完成此题,可以依据已有的知识进行,所以要求同学们在平时的学习中加强基础知识的记忆和理解,以便能够灵活应用.

练习册系列答案
相关题目
14.某化学兴趣小组学习氢氧化钠的性质之后展开探究性学习,请你作为该小组成员一起来解决下列问题;
(1)小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)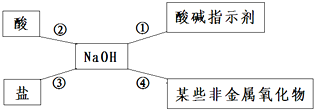
I.依据反应④说明,NaOH必须密封保存,否则在空气中要变质;其化学反应方程式为CO2+2NaOH=Na2CO3+H2O
II.为了验证反应③能够发生,你选择的物质是c(填序号).
a.Na2CO3 b. HCl c.CuSO4 d. Ba(NO3)2
(2)氢氧化钠溶液能使无色酚酞溶液变红色,且其中含有H2O、Na+、OH-三种微粒,小组同学想进一步探究是哪种微粒使无色酚酞溶液变红色.
【提出猜想】猜想①:可能是H2O;
猜想②:可能是Na+;
猜想③:可能是OH-.
【实验验证】
【讨论反思】有同学认为猜想①不需要实验验证就可以排除,你认为该同学的理由是无色酚酞试液中有大量水分子,已经证明水分子不能使酚酞变红色.
(1)小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)

I.依据反应④说明,NaOH必须密封保存,否则在空气中要变质;其化学反应方程式为CO2+2NaOH=Na2CO3+H2O
II.为了验证反应③能够发生,你选择的物质是c(填序号).
a.Na2CO3 b. HCl c.CuSO4 d. Ba(NO3)2
(2)氢氧化钠溶液能使无色酚酞溶液变红色,且其中含有H2O、Na+、OH-三种微粒,小组同学想进一步探究是哪种微粒使无色酚酞溶液变红色.
【提出猜想】猜想①:可能是H2O;
猜想②:可能是Na+;
猜想③:可能是OH-.
【实验验证】
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| ①用试管取少量蒸馏水,滴入1-2滴无色酚酞试液,振荡 | 试管内溶液仍为无色 | 水分子不能使无色酚酞试液变红色 |
| ②用试管取少量氯化钠溶液,滴入1-2滴无色酚酞试液,振荡 | 振荡试管内溶液仍为无色 | Na+不能使无色酚酞试液变红色 |
| ③用试管取少量氢氧化钠溶液,滴入1-2滴无色酚酞试液,振荡 | 试管内溶液变为红色 |
11. 某学习小组在探究酸的化学性质时,做了如图所示的两个实验:
某学习小组在探究酸的化学性质时,做了如图所示的两个实验:
(1)分别向两支装有碳酸钠和碳酸钙粉末的试管中注入一定量的稀盐酸,两支试管内均观察到的现象是有气泡产生,固体粉末全部消失,最终形成无色溶液.实验结束后,同学们将A、B两支试管中的废液倒入同一只洁净的烧杯中,发现烧杯中的废液变浑浊.写出产生浑浊现象的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)小组同学将烧杯中的物质进行了过滤,对滤液中的溶质成分展开了探究,请你一起参与.
【提出猜想】猜想1:滤液中的溶质是氯化钠;
猜想2:滤液中的溶质是氯化钠和碳酸钠;
猜想3:滤液中的溶质是氯化钠和氯化钙.
【设计实验】请你对猜想2进行验证.
 某学习小组在探究酸的化学性质时,做了如图所示的两个实验:
某学习小组在探究酸的化学性质时,做了如图所示的两个实验:(1)分别向两支装有碳酸钠和碳酸钙粉末的试管中注入一定量的稀盐酸,两支试管内均观察到的现象是有气泡产生,固体粉末全部消失,最终形成无色溶液.实验结束后,同学们将A、B两支试管中的废液倒入同一只洁净的烧杯中,发现烧杯中的废液变浑浊.写出产生浑浊现象的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)小组同学将烧杯中的物质进行了过滤,对滤液中的溶质成分展开了探究,请你一起参与.
【提出猜想】猜想1:滤液中的溶质是氯化钠;
猜想2:滤液中的溶质是氯化钠和碳酸钠;
猜想3:滤液中的溶质是氯化钠和氯化钙.
【设计实验】请你对猜想2进行验证.
| 实验步骤 | 预计实验现象 | 预计结论 |
| 取少量溶液于试管中, 加入少量的稀盐酸 | 产生气泡 | 猜想2正确 |
8.经过一年的化学学习,你认为下列认识或做法正确的是( )
| A. | 液化气被压缩到钢瓶是分子大小不变、间隔缩小 | |
| B. | 夏天比冬天食物更容易变质与氧气有关 | |
| C. | 晚上煤气泄漏时一定要及时开灯检查 | |
| D. | 经常用钢丝球洗刷铝锅可延长使用寿命 |
15.用于家庭装修的白色涂料中常添加二氧化钛(TiO2),其中Ti的化合价为( )
| A. | +2 | B. | +4 | C. | -2 | D. | -4 |
13.如图是四位同学正在讨论某一化学方程式表示的意义,他们所描述的化学方程式是( ) 

| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | ||
| C. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | D. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 |
