题目内容
7.要增大硝酸钾的溶解度,应采用的方法是( )| A. | 增加溶剂质量 | B. | 增加硝酸钾质量 | C. | 不断搅拌 | D. | 升高温度 |
分析 固体的溶解度受到温度和溶质、溶质性质的影响,而与溶质、溶剂的质量无关,更不会与搅拌与否有关了.
解答 解:
溶解度是物质的物理性质,与是否溶解,是否饱和无关,只受到温度以及溶质和溶剂的性质影响.
A、增加溶剂,会使饱和变成不饱和,而不饱和的则更不饱和,却无法改变溶解度.错误
B、增加溶质能够改变溶液是否饱和状态,但是不能改变溶解度大小.错误
C、搅拌能够加速溶质的溶解但是无法改变溶液是否饱和的状态,更不会改变溶质的溶解度.错误
D、升高温度,温度无论升高还是降低都会改变物质的溶解度.正确
故选D.
点评 溶解度属于物质的物理性质,与是否饱和无关,受到温度以及溶质、溶剂的性质的共同影响.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
13. 同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
【推理假设】
上述两种物质发生反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑,由此推测出废液中一定有NaCl,可能有Na2CO3或盐酸.
【实验探究】
(1)确定废液中是否含有盐酸
①选择试剂:根据盐酸的化学性质,同学们选用了如图所示的物种物质,其中物质X是酸碱指示剂中的石蕊溶液.
②实验验证:某同学向废液中加入少量的镁粉,观察到废液中无气泡产生,确定废液中一定没有盐酸.
(2)确定废液中是否含有Na2CO3:某同学选用pH试纸测出废液的pH=10,确定废液中一定含有Na2CO3.
(3)处理废液,回收利用,:欲从废液中得到纯净的NaCl,请完成如下实验方案设计.
(4)拓展运用:
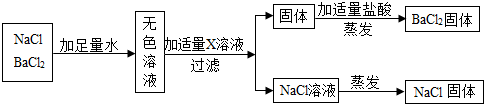
按照如图方案分离BaCl2和NaCl的固体混合物时,X溶液中溶质是溶质是Na2CO3.
 同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.【推理假设】
上述两种物质发生反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑,由此推测出废液中一定有NaCl,可能有Na2CO3或盐酸.
【实验探究】
(1)确定废液中是否含有盐酸
①选择试剂:根据盐酸的化学性质,同学们选用了如图所示的物种物质,其中物质X是酸碱指示剂中的石蕊溶液.
②实验验证:某同学向废液中加入少量的镁粉,观察到废液中无气泡产生,确定废液中一定没有盐酸.
(2)确定废液中是否含有Na2CO3:某同学选用pH试纸测出废液的pH=10,确定废液中一定含有Na2CO3.
(3)处理废液,回收利用,:欲从废液中得到纯净的NaCl,请完成如下实验方案设计.
| 方案 | 加入试剂 | 分离方法 | 方案评价 |
| 一 | 适量Ca(NO3)2溶液 | 过滤、蒸发结晶 | 不可行 |
| 二 | 过量的盐酸 | 蒸发结晶 | 可行 |
按照如图方案分离BaCl2和NaCl的固体混合物时,X溶液中溶质是溶质是Na2CO3.

12.现有一包白色粉末,可能由NaCl、Na2SO4中的一种或两种组成,小科为了确定该粉末的组成,取少量粉末按如图所示进行实验,在AgNO3、Ba(NO3)2、BaCl2溶液中选择两种作为A、B试剂,且A、B的阳离子不同,结果鉴别出了该粉末的组成,则下列说法正确的是( )


| A. | 原粉末只含NaCl | |
| B. | 原粉末只含Na2SO4 | |
| C. | 试剂B可能是Ba(NO3)2溶液 | |
| D. | 试剂A选Ba(NO3)2溶液或BaCl2溶液均可 |
16.判别下列物质全部属于有机化合物的是( )
| A. | 碳酸钙、甲烷、淀粉 | B. | 碳酸钠、油、蛋白质 | ||
| C. | 酒精、二氧化碳、葡萄糖 | D. | 甲烷、蔗糖、脂肪 |
 许多化学反应都伴随着明显的现象.但也有一些观察不到明显现象.请回答问题:
许多化学反应都伴随着明显的现象.但也有一些观察不到明显现象.请回答问题: