题目内容
取30克3.4%的过氧化氢溶液制取氧气,为了加快反应实验中加入了1克二氧化锰.①该实验中二氧化锰的作用是______.
②该溶液中过氧化氢的物质的量是______.
③可制得氧气的物质的量______(根据化学方程式计算).
【答案】分析:①依据二氧化锰是该反应的催化剂分析解答;
②利用溶液的有关计算求出过氧化氢溶液过氧化氢的质量,而后利用物质的质量与物质的量之间的有关计算分析解答;
③利用化学方程式的有关计算解答即可;
解答:解:①由于二氧化锰是该反应的催化剂,故二氧化锰的作用是催化作用;
②30克3.4%的过氧化氢溶液中过氧化氢的质量是30g×3.4%=1.02g,故该溶液中过氧化氢的物质的量是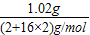 =0.03mol;
=0.03mol;
③设可以制得的氧气物质的量是x
2H2O2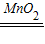 2H2O+O2↑
2H2O+O2↑
2 1
0.03mol x
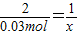
x=0.015mol
故答案为:①催化作用;②0.03mol;③0.015mol;
点评:此题是对溶液以及化学方程式计算的考查,解题的关键是掌握物质的质量与物质的量之间的转化关系;
②利用溶液的有关计算求出过氧化氢溶液过氧化氢的质量,而后利用物质的质量与物质的量之间的有关计算分析解答;
③利用化学方程式的有关计算解答即可;
解答:解:①由于二氧化锰是该反应的催化剂,故二氧化锰的作用是催化作用;
②30克3.4%的过氧化氢溶液中过氧化氢的质量是30g×3.4%=1.02g,故该溶液中过氧化氢的物质的量是
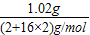 =0.03mol;
=0.03mol;③设可以制得的氧气物质的量是x
2H2O2
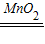 2H2O+O2↑
2H2O+O2↑2 1
0.03mol x
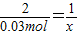
x=0.015mol
故答案为:①催化作用;②0.03mol;③0.015mol;
点评:此题是对溶液以及化学方程式计算的考查,解题的关键是掌握物质的质量与物质的量之间的转化关系;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目