题目内容
16.下列曲线示意图与相应选项表示不正确的是( )| A. |  表示稀盐酸中滴加蒸馏水 表示稀盐酸中滴加蒸馏水 | |
| B. |  表示等体积、等质量分数的过氧化氢溶液分解 表示等体积、等质量分数的过氧化氢溶液分解 | |
| C. |  表示质量、颗粒大小都相等的金属加到等质量等质量分数量且足量的稀盐酸中 表示质量、颗粒大小都相等的金属加到等质量等质量分数量且足量的稀盐酸中 | |
| D. |  表示H2SO4和CuSO4的混合溶液中滴加Ba(OH)2溶液 表示H2SO4和CuSO4的混合溶液中滴加Ba(OH)2溶液 |
分析 根据已有的物质的反应以及与图象的关系进行分析解答即可.
解答 解:A、表示稀盐酸中滴加蒸馏水,则溶液的pH逐渐增大,但是不会大于等于7,正确;
B、等体积、等质量分数的过氧化氢溶液分解,加二氧化锰的反应快,不加二氧化锰的反应慢,正确;
C、质量、颗粒大小都相等的金属加到等质量等质量分数量且足量的稀盐酸中,由于镁的活动性强于铁,故镁反应的快,由于镁反应生成的氢气的质量大于铁,故图象正确;
D、H2SO4和CuSO4的混合溶液中滴加Ba(OH)2溶液,开始就会产生沉淀,不会过一段时间出现沉淀,错误;
故选D.
点评 本题考查的是常见的化学反应以及反应过程中有关的量的图象,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
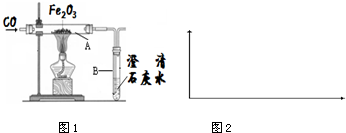
6.某化学兴趣小组如图1模拟教材中的炼铁实验,再将所得的黑色粉末物质与足量的稀硫酸反应,发现黑色粉末消失,但始终没有气泡生成.
(1)铁元素的常见价态有+2、+3.将Fe3O4表示为两种氧化物的结合形式FeO•Fe2O3.
(2)根据现象“没有气泡生成”猜想,黑色粉末物质可能是:
①氧化亚铁;②四氧化三铁;③氧化亚铁和四氧化三铁的混合物.
(3)图中装置有明显缺陷,从环保角度出发,应采取的措施是将尾气点燃.
(4)从实验安全角度考虑,应在装置A、B间增加一个安全瓶,可以有效防止B中的澄清石灰水倒吸入A中.
(5)某科技小组查阅CO与Fe2O3反应各产物开始生成的温度情况:
Fe2O3$\stackrel{300℃以上}{→}$Fe3O4$\stackrel{600℃以上}{→}$FeO$\stackrel{700℃以上}{→}$Fe
由于酒精灯通常只能提供400-500℃的温度,则黑色粉末的成分理论上可确定为Fe3O4.
(6)设计实验对黑色粉末进行探究.
某同学选用X溶液与黑色粉末反应,也可以证明黑色粉末中不含有Fe,则X为A.
A.硫酸铜溶液 B.硫酸钠溶液 C.氢氧化钠溶液 D.氢氧化钙溶液
(7)在一定温度下,该科研小组将3.2克Fe2O3与足量的CO混合加热,反应结束后冷却,精确称量黑色粉末质量为ag(计算保留两位有效数字)
①若a=2.24g,黑色粉末是Fe;②若a=2.88g,黑色粉末是FeO;③若a=3.09g,黑色粉末是Fe3O4;
④若黑色粉末是混合物则a的取值范围是2.24g<a<3.09g.
(8)请你画出以温度为横坐标,玻璃管中剩余固体的质量为纵坐标(如图2),表示用CO还原Fe2O3.

(1)铁元素的常见价态有+2、+3.将Fe3O4表示为两种氧化物的结合形式FeO•Fe2O3.
(2)根据现象“没有气泡生成”猜想,黑色粉末物质可能是:
①氧化亚铁;②四氧化三铁;③氧化亚铁和四氧化三铁的混合物.
(3)图中装置有明显缺陷,从环保角度出发,应采取的措施是将尾气点燃.
(4)从实验安全角度考虑,应在装置A、B间增加一个安全瓶,可以有效防止B中的澄清石灰水倒吸入A中.
(5)某科技小组查阅CO与Fe2O3反应各产物开始生成的温度情况:
Fe2O3$\stackrel{300℃以上}{→}$Fe3O4$\stackrel{600℃以上}{→}$FeO$\stackrel{700℃以上}{→}$Fe
由于酒精灯通常只能提供400-500℃的温度,则黑色粉末的成分理论上可确定为Fe3O4.
(6)设计实验对黑色粉末进行探究.
| 操作步骤 | 实验现象 | 解释或反应方程式 |
| 1.取少量黑色物质加入 30%热的盐酸中 | 无气泡、溶液颜 色变成黄绿色 | 该反应的化学方程式:Fe3O4+8HCl═FeCl2+2FeCl3+4H2O |
| 2.用磁铁吸引此粉末 | 能够被吸引 | 说明该物质具有磁性 |
A.硫酸铜溶液 B.硫酸钠溶液 C.氢氧化钠溶液 D.氢氧化钙溶液
(7)在一定温度下,该科研小组将3.2克Fe2O3与足量的CO混合加热,反应结束后冷却,精确称量黑色粉末质量为ag(计算保留两位有效数字)
①若a=2.24g,黑色粉末是Fe;②若a=2.88g,黑色粉末是FeO;③若a=3.09g,黑色粉末是Fe3O4;
④若黑色粉末是混合物则a的取值范围是2.24g<a<3.09g.
(8)请你画出以温度为横坐标,玻璃管中剩余固体的质量为纵坐标(如图2),表示用CO还原Fe2O3.
7.下列各组内物质的溶液混合后,所得溶液一定呈碱性的是( )
| A. | KOH、Na2CO3、HCl | B. | BaCl2、NaCl、H2SO4 | ||
| C. | Ca(OH)2、KNO3、Na2CO3 | D. | Ba(OH)2、NaOH、HNO3 |
1.下列实验现象描述正确的是( )
| A. | 红磷燃烧产生大量的白色烟雾 | |
| B. | 向硫酸铜溶液中滴加NaOH溶液生成白色沉淀 | |
| C. | 将除去铁锈的铁钉放入到稀盐酸中,铁钉表面产生气泡,溶液变为黄色 | |
| D. | 将CO2通入到紫色的石蕊试液中,试液变为红色 |
5.将金属钠放入燃烧匙,点燃后伸入氯气瓶中,生成氯化钠.有关此反应描述正确的是( )
| A. | 钠原子得到电子变成阳离子 | |
| B. | 氯气中氯元素的化合价为-1价 | |
| C. | 反应前后钠元素总质量不变 | |
| D. | 氯化钠由氯元素和钠元素组成,所以是混合物 |
6.某化学兴趣小组设计四种实验方案来证明炭粉中是否含有氧化铜.其中可行的是( )
| A. | 将固体高温加热,看是否有红色固体生成 | |
| B. | 在样品中加稀硫酸,充分反应后,观察是否有固体剩余 | |
| C. | 在样品中加水,是否有蓝色沉淀 | |
| D. | 在样品中加硫酸,充分反应后,溶液是否呈蓝色 |