题目内容
16.实验室有一瓶久置的初中化学常用的无色溶液,其残缺的标签中只剩下“Na”和“10%”等字样,小昊和小宇同学对此很感兴趣,决定探究其成分.【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A.
A.酸 B.碱 C.盐
【查阅资料】
①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
②Na2CO3和NaHCO3溶液呈碱性.
③测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【实验探究】
(1)小宇用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得PH>7,这瓶试剂不可能是NaCl.
(2)小昊为了确定该溶液是哪种溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 稀盐酸 | 产生大量的气泡 | 该溶液是Na2CO3,反应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑. |
【反思与评价】小飞认为由于试剂久置,上述探究得到的结论不可靠,他的理由是(用化学方程式表示)2NaOH+CO2═Na2CO3+H2O.
分析 【交流讨论】根据酸、碱、盐的组成特点及标签可见部分,猜测该溶液不可能属于哪类物质的溶液;
【理论探讨】根据溶液中溶质溶解度与饱和溶液中溶质的质量分数的关系,由常温下各物质的溶解度及该溶液中溶质质量分数,判断溶液的可能性;
【实验探究】(1)根据三种物质溶液的酸碱性及所测定溶液的酸碱度,对溶液的可能做出判断;
(2)利用碳酸钠、氢氧化钠性质差异及所设计实验中的现象,判断所采取的鉴别所用试剂、现象及结论;
【拓展与应用】根据碳酸钠、氢氧化钠的性质差异,另选一种试剂完成两种物质的鉴别;
【反思与评价】根据氢氧化钠的性质分析.
解答 解:【交流讨论】破损标签可见部分为钠元素,可判断该物质由金属元素与根组成,而酸类物质由氢元素与酸根所组成,可判断该物质不可能为酸;
【理论探讨】常温下碳酸氢钠的溶液为9.6g,可判断常温下碳酸氢钠的饱和溶液的溶质质量分数=$\frac{9.6g}{100g+9.6g}$×100%=8.8%<10%,因此可判断该溶液不可能为碳酸氢钠溶液;
【实验探究】(1)由于氢氧化钠、碳酸钠溶液都为碱性,pH>7,而氯化钠为中性,pH=7,因此不可能是氯化钠溶液;
(2)根据碳酸钠能与盐酸反应放出二氧化碳而氢氧化钠与盐酸反应无明显现象,因此,可推断鉴别两物质时所加入的试剂为稀盐酸,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,观察有气泡可说明该物质为碳酸钠,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
【拓展与应用】利用氢氧化钙(或氢氧化钡)能与碳酸钠反应生成白色碳酸钙沉淀(或碳酸钡沉淀),因此可使用氢氧化钙溶液(或氢氧化钡溶液)鉴别NaOH溶液和Na2CO3溶液;也可用氯化钙溶液或氯化钡溶液进行鉴别,现象相同;
【反思与评价】因为氢氧化钠放置较长时间会产生碳酸钠,因此碳酸钠可能是氢氧化钠变质产生的,加入稀盐酸也会产生气体;
故答案为:【交流讨论】A;
【理论探讨】NaHCO3;
【实验探究】
(1)NaCl;
(2)稀盐酸;Na2CO3;Na2CO3+2HCl═2NaCl+H2O+CO2↑;
【拓展与应用】氢氧化钙溶液,产生白色沉淀;
【反思与评价】2NaOH+CO2═Na2CO3+H2O.
点评 本题综合利用了物质的组成、物质的溶解性、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,充分体现了运用化学知识分析问题、解决问题的能力,是一道不错的题目.

| A. | 利用洗衣液的乳化作用可以去除衣物上的油污 | |
| B. | 可以用锅、红磷、木炭除去空气中氧气来测定空气中氧气的含量 | |
| C. | 铝粉能在空气中剧烈燃烧,生成黑色的氧化铝 | |
| D. | 粉尘爆炸属于缓慢氧化反应 |

| A. | X是稀盐酸 | B. | Y是水 | ||
| C. | Z是石灰水 | D. | X与Z反应会生成Y,这属于化合反应 |
| A. | 食用蔬菜、水果可以补充维生素 | |
| B. | 隔绝氧气和水可以防止铁制品生锈 | |
| C. | 汽车安装尾气净化装置可以节约石油资源 | |
| D. | 工厂废水处理后循环使用可以节约水资源 |
实验室用石灰水而不用氢氧化钠溶液鉴定二氧化碳。氢氧化钠能否与二氧化碳反应?
【查阅资料】Ⅰ.氢氧化钠溶液与二氧化碳反应生成易溶的碳酸钠,碳酸钠在二氧化碳过量的条件下继续与水和二氧化碳反应生成碳酸氢钠
Ⅱ.碳酸钠和碳酸氢钠性质对比如下表
操作 | NaHCO3溶液 | Na2CO3溶液 |
加入稀盐酸 | 产生气泡 | 产生气泡 |
加入稀CaCl2溶液 | 无明显变化 | __________________(填写现象)) |
加热溶液至沸腾,并将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
【进行实验】
实验操作 | 实验现象 | 结论及化学方程式 |
| ___________________ | 氢氧化钠与二氧化碳反应生成碳酸钠.反应方程式_______________ |
【实验反思】学习小组讨论,认为产生此实验现象的原因可能有两种:一种是NaOH与C02发生了反应;另一种是_______________
(2)为了进一步验证CO2与NaOH溶液已经发生反应,请你设计一个简单的实验检验生成的新物质。
实验步骤 | 实验现象 | 解释与结论 |
____________________________ | ____________________________ | NaOH与CO2发生了反应 |
【实验拓展】该小组同学将二氧化碳通入氢氧化钠溶液中,利用数字化技术测定溶液pH值变化,待完全反应后,观察到溶液中逸出大量气泡,pH出现两段S型变化曲线。

【实验分析】
(3)AB段变化的原因可能是________。BC段变化的原因可能是___________。利用实验验证变化后的产物,实验操作为_________________.实验现象是____________________。
南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为“504双吸剂”,其标签如下图所示。南南和北北对这包久置的“504双吸剂”固体样品很好奇,设计如下实验进行探究。

【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
【实验探究】南南同学的方案:
实验操作 | 实验现象 | 实验结论 |
取少量固体放于试管中,滴加足量的 。 | 固体逐渐消失,有无色气体产生,得到浅绿色溶液。 | 固体中一定含有 , 一定不含Fe2O3。 |
北北同学认为南南同学的实验并不能得出一定不含Fe2O3的结论,理由是 ,并设计如下实验方案继续验证。

(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是 。
(2)步骤②中固体溶解时放出大量热,由此可以判断固体中一定含有 。写出该过程中的化学方程式 。
(3)步骤③中反应的化学方程式是 。
北北同学对滤渣B又进行探究。
实验操作 | 实验现象 | 实验结论 |
① 取滤渣B于试管中,加入适量 ② 生成的气体通入 | ① ②该溶液变浑浊。 | 固体中一定含有CaCO3 和Fe2O3。 |
【实验结论】综合上述实验及所给数据,该久置固体中一定含有的物质是Fe、Fe2O3、CaO、CaCO3。
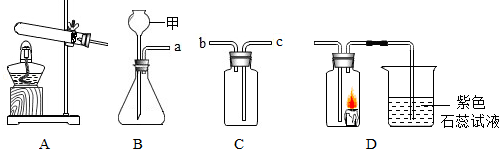

 塞紧橡皮塞 B.
塞紧橡皮塞 B.  加热液体 C.
加热液体 C.  取用液体 D.
取用液体 D.  读出液体的体积
读出液体的体积