题目内容
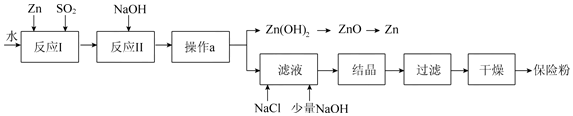
1. 小甜利用石灰石和稀盐酸进行如下实验,操作过程和数据如图所示(样品中的杂质不与酸反应也不溶于水).
小甜利用石灰石和稀盐酸进行如下实验,操作过程和数据如图所示(样品中的杂质不与酸反应也不溶于水).(1)20g石灰石样品中CaCO3的质量为15g.
(2)列式计算不饱和溶液A的溶质质量分数(结果准确到0.1%).
分析 (1)根据碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,样品中的杂质不与酸反应也不溶于水分析;
(2)根据碳酸钙的质量结合化学方程式计算反应后生成氯化钙的质量,进一步计算计算不饱和溶液A的溶质质量分数.
解答 解:(1)根据碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,样品中的杂质不与酸反应也不溶于,所以恰好反应后剩余的固体为杂质,20g石灰石样品中CaCO3的质量为20g-5g=15g;故填:15;
(2)设生成氯化钙的质量为x,生成二氧化碳的质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
15g x y
$\frac{100}{15g}=\frac{111}{x}=\frac{44}{y}$
x=16.65g,y=6.6g
不饱和溶液A的溶质质量分数为$\frac{16.65g}{15g+100g-6.6g}×100%$=15.4%.
答:不饱和溶液A的溶质质量分数为15.4%.
点评 本题是运用化学中的基本思想质量守恒思想,通过分析发生的化学反应原理推知碳酸钙的质量,并进行方程式计算,从而培养了学生的分析、解决问题的能力.

练习册系列答案
相关题目
11.下列化肥分别与熟石灰混合研磨后.能闻到刺激性气味的是( )
| A. | NH4Cl | B. | KNO3 | C. | NaNO3 | D. | Ca3(PO4)2 |
12.下列说法中正确的是( )
| A. | 检验电解水的产物,可判断水的组成元素 | |
| B. | 将pH试纸用水润湿后,测定柠檬汁的pH | |
| C. | 凡是无色的、均一的液体一定是溶液 | |
| D. | 硫在O2中燃烧发出淡蓝色火焰,生成SO3 |
9.下列物质溶于水时,溶液温度明显下降的是( )
| A. | 食盐 | B. | 浓硫酸 | C. | 硝酸铵 | D. | 氢氧化钠 |
16.物质的性质决定用途.下列是物质的一些性质:①密度小,很稳定、②有吸附性、③有导电性、④易升华、⑤能与酸反应.请选择恰当的数字序号填空.
| 用途 |  石墨作电极芯 |  活性炭用于防毒面具 |  氦气用于探空气球 |  碳酸氢钠用于面点发酵 |  干冰用于人工降雨 |
| 性质 | (1)石墨具有导电性 | (2)活性炭具有吸附性 | (3)氦气密度比空气小 | (4)碳酸氢钠受热易分解 | (5)干冰易升华,吸收大量的热 |
5.下列除去杂质的方法中,不正确的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | 铜粉(铁粉) | 加入足量稀硫酸,过滤、洗涤、干燥 |
| B | CO(CO2) | 通过足量的NaOH溶液,干燥 |
| C | CaCl2溶液(HCl) | 加过量的碳酸钙,过滤 |
| D | NaNO3溶液(Na2CO3) | 加入过量的Ba(NO3)2溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
9.下列化学用语书写正确的是( )
| A. | 氮分子N | B. | 4个氢原子2H2 | C. | 铵根离子NH4+ | D. | 氧化铁FeO |
10.对暴露在空气中部分变质的氢氧化钠溶液(以下简称样品)进行如下的四个实验,其中叙述错误的是( )
| A. | 向样品中滴入澄清石灰水,有白色沉淀生成 | |
| B. | 向样品中滴入足量的稀盐酸,有气体产生 | |
| C. | 除去样品中的杂质,可以加入过量石灰水,充分反应后再过滤 | |
| D. | 先向样品中加入足量CaCl2溶液,充分反应后滴加酚酞试液,上层清液变红色 |