题目内容
某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0g石灰石样品,把25.0g稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
请计算:
(1)确定上表中x的值为 ;
(2)石灰石样品中碳酸钙的质量分数为 .
(3)稀盐酸中溶质的质量分数是多少?
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g | x |
(1)确定上表中x的值为
(2)石灰石样品中碳酸钙的质量分数为
(3)稀盐酸中溶质的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)由实验数据表可知,每加入5g稀盐酸,与碳酸钙物质完全反应,剩余固体减少0.5g,即每次参加反应的碳酸钙的质量为0.5g;前三次实验中盐酸均完全反应,而第四次加入5g稀盐酸,固体的质量减少=0.5g-0.3g=0.2g,说明碳酸钙已经完全反应,剩余0.3g为杂质的质量,所以第5次再加入盐酸,固体的质量不变进行解答;
(2)由石灰石样品中碳酸钙的质量可以计算出碳酸钙的质量分数.
(3)根据题意,利用样品中的碳酸钙质量,据此根据反应的化学方程式计算所用稀盐酸中溶质的质量,进而由溶质的质量分数的计算方法计算出质量分数即可.
(2)由石灰石样品中碳酸钙的质量可以计算出碳酸钙的质量分数.
(3)根据题意,利用样品中的碳酸钙质量,据此根据反应的化学方程式计算所用稀盐酸中溶质的质量,进而由溶质的质量分数的计算方法计算出质量分数即可.
解答:解:(1)由实验数据表可知,每加入5g稀盐酸,与碳酸钙物质完全反应,剩余固体减少0.5g,即每次参加反应的碳酸钙的质量为0.5g;前三次实验中盐酸均完全反应,而第四次加入5g稀盐酸,固体的质量减少=0.5g-0.3g=0.2g,说明碳酸钙已经完全反应,剩余0.3g为杂质的质量,所以第5次再加入盐酸,固体的质量不变,所以表中x的值为0.3;故填:0.3;
(2)该石灰石样品中含碳酸钙质量=2g-0.3g=1.7g,
石灰石样品中碳酸钙的质量分数=
×100%=85%;故填:85%;
(3)设参加反应的5g稀盐酸中HCl质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
0.5g x
=
x=0.365g
稀盐酸中溶质的质量分数=
×100%=7.3%.
答:所用稀盐酸中溶质的质量分数为7.3%.
(2)该石灰石样品中含碳酸钙质量=2g-0.3g=1.7g,
石灰石样品中碳酸钙的质量分数=
| 1.7g |
| 2g |
(3)设参加反应的5g稀盐酸中HCl质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
0.5g x
| 100 |
| 0.5g |
| 73 |
| x |
x=0.365g
稀盐酸中溶质的质量分数=
| 0.365g |
| 5g |
答:所用稀盐酸中溶质的质量分数为7.3%.
点评:本题难度较大,考查了根据化学方程式的计算,根据表格数据分析出石灰石样品中的碳酸钙与稀盐酸恰好完全反应的实验是正确解答本题的关键所在.

练习册系列答案
相关题目
化学反应2Al+3CuSO4═3Cu+Al2(SO4)3,该反应的基本反应类型是( )
| A、化合反应 | B、分解反应 |
| C、置换反应 | D、复分解反应 |
 在用稀盐酸和氢氧化钡溶液进行中和反应实验时,反应过程中溶液酸碱度变化及相关数
在用稀盐酸和氢氧化钡溶液进行中和反应实验时,反应过程中溶液酸碱度变化及相关数 日本福岛核电站发生核泄漏,增加了空气中的放射线碘131和铯137等元素.碘的原子结构示意图如图:
日本福岛核电站发生核泄漏,增加了空气中的放射线碘131和铯137等元素.碘的原子结构示意图如图: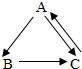 A、B、C是初中常见的三种白色固体,它们的转化关系如右图所示(部分物质已略去),其中A的相对分子质量为100,B是常用的干燥剂,C是氯化物.请写出B的俗名
A、B、C是初中常见的三种白色固体,它们的转化关系如右图所示(部分物质已略去),其中A的相对分子质量为100,B是常用的干燥剂,C是氯化物.请写出B的俗名 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如右图所示.问:
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如右图所示.问: 华雪同学对氯化镁固体样品(仅含杂质NaCl)进行如下检测:取5.0g样品溶于一定量的水中得到25.0g溶液,再加入溶质质量分数为10%的氢氧化钠溶液,实验时得到沉淀的质量与加入NaOH溶液的质量关系如图所示:
华雪同学对氯化镁固体样品(仅含杂质NaCl)进行如下检测:取5.0g样品溶于一定量的水中得到25.0g溶液,再加入溶质质量分数为10%的氢氧化钠溶液,实验时得到沉淀的质量与加入NaOH溶液的质量关系如图所示: