题目内容
1.下表是硝酸钾和氯化铵在不同温度时的溶解度.分析表中数据,回答问题.| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | |
(2)60℃时,两种物质的饱和溶液中,溶质质量分数较小的是氯化铵.
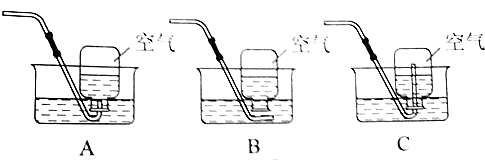
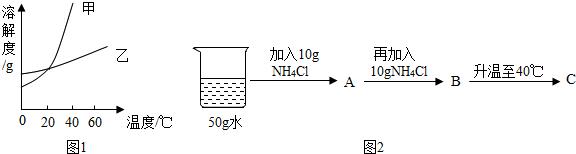
(3)20℃时,按图2所示操作:B中的溶液是饱和(选填“饱和”或“不饱和”)溶液,C中溶液的溶质和溶剂质量比为2:5.(填最简整数比)
(4)20℃时,甲的饱和溶液升温至60℃(不考虑蒸发),则甲溶液溶质的质量分数将不变(填“变大”“变小”“不变”之一).
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度表中的数据可知,硝酸钾的溶解度受温度影响较大,所以甲可表示硝酸钾的溶解度曲线;
(2)60℃时,氯化铵的溶解度较小,所以两种物质的饱和溶液中,溶质质量分数较小的是氯化铵;
(3)20℃时,氯化铵的溶解度是37.2g,按图2所示操作:B中的溶液是饱和溶液,20℃时,氯化铵的溶解度是55.2g,所以C中溶液的溶质和溶剂质量比为2:5;
(4)甲物质的溶解度随温度的升高而增大,所以20℃时,甲的饱和溶液升温至60℃(不考虑蒸发),则甲溶液溶质的质量分数将不变.
故答案为:(1)硝酸钾;
(2)氯化铵;
(3)饱和,2:5;
(4)不变.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
6.正确的实验操作是科学探究成功的基础.下列操作中正确的是( )
| A. |  滴瓶滴管使用 滴瓶滴管使用 | B. |  塞紧橡皮塞 塞紧橡皮塞 | C. |  测量溶液的PH 测量溶液的PH | D. |  闻气体气味 闻气体气味 |
13.如图四个图象能正确反映对应实验操作的是( )
| A. |  向一定量的氢氧化钠和氯化钡混合溶液中不断滴入稀硫酸 | |
| B. | 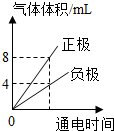 加有Na2SO4的蒸馏水通电 加有Na2SO4的蒸馏水通电 | |
| C. | 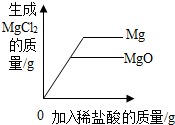 向等质量的Mg和MgO中分别加入足量等浓度的稀盐酸 | |
| D. | 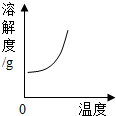 一定压强下,氧气在水中的溶解度 |
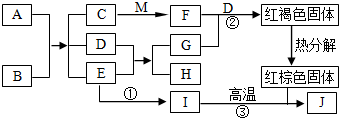
 如图为某医用葡萄糖注射液标签的一部分.
如图为某医用葡萄糖注射液标签的一部分.