题目内容
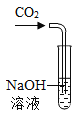
【题目】.某化学兴趣小组的同学研究CO2通入NaOH溶液是否发生反应,他们设计了以下实验。请你参与他们的探究活动,并回答有关问题。
(设计与实验)
实验序号 | 步骤一 | 步骤二 |
实验Ⅰ |
|
|
实验Ⅱ |
|
|
(探究与结论)
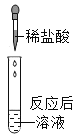
(1)实验I的步骤二中产生的实验现象是_________,反应的化学方程式为_______________。
(2)实验Ⅱ的步骤二中产生的实验现象是_____________。
(3)在实验I、实验Ⅱ的步骤一中,CO2和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是______________。
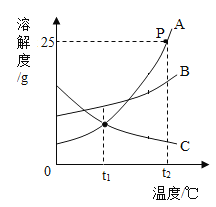
(拓展延伸)已知20℃时NaOH、Na2CO3在水中和酒精中的溶解度如下:
在水中的溶解度/g | 在酒精中的溶解度/g | |
NaOH | 109 | 17.3 |
Na2CO3 | 21.8 | <0.01 |
请利用以上信息设计实验Ⅲ,证明CO2确实与NaOH发生了化学反应。
(1)用化学方程式表示实验Ⅲ的原理:____________________。
(2)实验Ⅲ的主要操作是_____________________。
(交流反思)通过实验I~Ⅲ可知,验证无明显现象的反应是否发生,可以采用检验生成物的方法。请你再列举一种检验方法:______。
【答案】有气泡冒出 ![]() 产生白色沉淀 CO2与无色的NaOH溶液反应生成无色的Na2CO3溶液
产生白色沉淀 CO2与无色的NaOH溶液反应生成无色的Na2CO3溶液 ![]() 将二氧化碳通入氢氧化钠的酒精溶液中 检验反应物是否减少
将二氧化碳通入氢氧化钠的酒精溶液中 检验反应物是否减少
【解析】
探究与结论:
实验I的步骤一中,二氧化碳通入NaOH溶液,反应生成碳酸钠和水,碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,故实验I的步骤二中产生的实验现象是有气泡冒出,反应的化学方程式为![]() 。
。
(2)实验Ⅱ的步骤二中有白色沉淀产生,因为碳酸钠溶液与氯化钙溶液反应生成碳酸钙沉淀,即![]() ,也间接证明CO2与NaOH溶液发生了反应。在实验I、实验Ⅱ的步骤一中,CO2和无色的NaOH溶液反应生成了无色的Na2CO3溶液,因而看不到明显现象。
,也间接证明CO2与NaOH溶液发生了反应。在实验I、实验Ⅱ的步骤一中,CO2和无色的NaOH溶液反应生成了无色的Na2CO3溶液,因而看不到明显现象。
拓展延伸:
根据题给信息可知,氢氧化钠在酒精中的溶解度较大,而碳酸钠在酒精中的溶解度很小。因此,若将二氧化碳气体通入氢氧化钠的酒精溶液中,生成的碳酸钠在酒精中难以溶解,因此就会观察到有白色沉淀生成,从而直接证明CO2与NaOH溶液发生了化学反应;
(1)反应的化学方程式为![]() 。
。
(2)实验Ⅲ的主要操作是将二氧化碳气体通入氢氧化钠的酒精溶液中。
交流反思:
还可以采用检验反应物是否减少的方法。

【题目】研究氢气的燃烧实验是人们认识水的组成的开始。实验室中常用锌粒和稀硫酸反应来制备氢气。查阅资料:浓硫酸可以吸水。
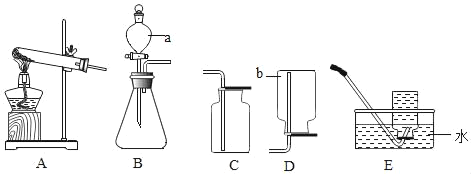
(1)仪器①的名称是_____;实验室制取氢气的发生装置是_____(填字母),要收集干燥的氢气,则氢气要从C装置中_____ (填“a”或“b”)管口进入。
(2)某化学兴趣小组的同学用“电解法”证明了水的组成,如图D所示,该装置中发生反应的基本类型是_____。打开活塞b,用燃着的木条在玻璃管尖嘴口检验反应产生的气体,看到的现象是_____。
(3)同学们查阅资料得知拉瓦锡用另一实验证明了水的组成。他让水蒸气通过一根高温烧红的铁质枪管,结果得到了氢气,同时枪管表面有黑色固体(四氧化三铁)生成。该反应的化学方程式为_____。
(继续探究)该兴趣小组的同学决定用氢气继续进行探究,他们取7支试管,依次盛水90%(体积分数)、80%……再用排水法收集氢气,而后分别把试管口移近酒精灯火焰,实验结果如表所示:
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
氢气体积分数(%) | 90 | 80 | 70 | 50 | 20 | 10 | 5 |
空气体积分数(%) | 10 | 20 | 30 | 50 | 80 | 90 | 95 |
点燃现象 | 安静燃烧 | 安静燃烧 | 弱的爆鸣声 | 强的爆鸣声 | 强的爆鸣声 | 弱的爆鸣声 | 不燃烧不爆鸣 |
分析表中信息,完成下列问题:
(4)在混合气体爆炸范围内,氢气的体积分数范围约为_____。
(5)你对燃烧或燃烧条件的新认识是_____。
【题目】如图是部分元素的离子结构示意图和元素周期表的一部分。请回答:
| ||||||
| ||||||
|
| |||||
(1)图①、②中属于阴离子的是______(填序号),该元素的质子数为______;13号元素原子的最外层电子数为______。

(2)由表中原子序数为1、8、13的元素组成物质的化学式为______。