题目内容
图1为实验室常用的实验装置,回答问题:
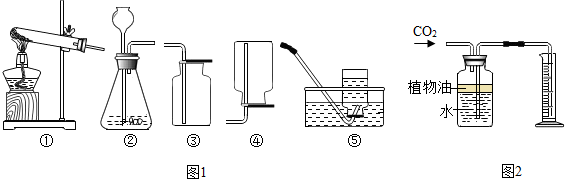
(1)用稀盐酸和石灰石反应制CO2,应选用的发生和收集装置是 (填序号).
(2)图2所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是 .
(3)实验室也可用加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,该反应的化学方程式 .

(1)用稀盐酸和石灰石反应制CO2,应选用的发生和收集装置是
(2)图2所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是
(3)实验室也可用加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,该反应的化学方程式
考点:二氧化碳的实验室制法,量气装置,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置;
(2)根据二氧化碳的性质能溶于水进行解答;
(3)加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,写出上述反应的化学方程式即可.
(2)根据二氧化碳的性质能溶于水进行解答;
(3)加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,写出上述反应的化学方程式即可.
解答:解:(1)用稀盐酸和石灰石制取二氧化碳,不需加热,属于固液常温型,故选B发生装置;二氧化碳的密度比空气大且溶于水,故可用向上排空气法收集;故填:②③;
(2)要测量二氧化碳的体积只能用排水法,用量筒测量水的体积从而测二氧化碳的体积,二氧化碳能溶于水,所以要在水的上方放一层植物油,以防止二氧化碳与水接触.故填:阻止二氧化碳与水接触;
(3)加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,该反应的化学方程式为:2NaHCO3
Na2CO3+H2O+CO2↑.故填:2NaHCO3
Na2CO3+H2O+CO2↑.
(2)要测量二氧化碳的体积只能用排水法,用量筒测量水的体积从而测二氧化碳的体积,二氧化碳能溶于水,所以要在水的上方放一层植物油,以防止二氧化碳与水接触.故填:阻止二氧化碳与水接触;
(3)加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,该反应的化学方程式为:2NaHCO3
| ||
| ||
点评:本题难度不是很大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据是正确解答本题的关键.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
属于分解反应的是( )
| A、Ca(HCO3)2→CaCO3↓+CO2↑+H2O |
| B、2Na+Cl2→2NaCl |
| C、2Mg+CO2→2MgO+C |
| D、AgNO3+NaCl→AgCl↓+NaNO3 |
下列微粒中,能保持氧气化学性质的是( )
| A、O |
| B、O2- |
| C、2O |
| D、O2 |
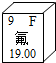 元素周期表是学习化学的重要工具,如图是摘自元素周期表中的一格,据此图能获得的信息是( )
元素周期表是学习化学的重要工具,如图是摘自元素周期表中的一格,据此图能获得的信息是( )| A、该元素的原子核内有9个中子 |
| B、该元素的原子核外有9个电子 |
| C、该元素在地壳中的含量为19.00% |
| D、该元素属于金属元素 |
下列说法正确的是( )
| A、熄灭酒精灯用嘴吹灭 |
| B、硫在空气中燃烧产生无色无味的气体 |
| C、做硫粉、细铁丝在氧气中燃烧实验时都要在集气瓶中装少量水,但水的作用不同 |
| D、二氧化硫是空气污染物,要控制其排放 |
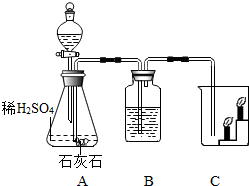 如图是实验室制取二氧化碳并试验其性质的装置.
如图是实验室制取二氧化碳并试验其性质的装置. 某同学将在黑暗中放置了24小时的两盆植物,分别移置在透明、密闭的玻璃装置中(如图甲、乙示),再放在阳光下照射4小时.然后各取一张叶子,经酒精煮沸脱色后滴碘液检验.
某同学将在黑暗中放置了24小时的两盆植物,分别移置在透明、密闭的玻璃装置中(如图甲、乙示),再放在阳光下照射4小时.然后各取一张叶子,经酒精煮沸脱色后滴碘液检验.