题目内容
20.如图中实验操作正确的是( )| A. | 闻气体气味 | B. | 取用块状固体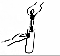 | C. | 滴加液体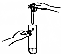 | D. | 加热液体 |
分析 A、根据闻气体的气味时的方法(招气入鼻法)进行分析判断.
B、根据向试管中装块状固体药品的方法进行分析判断.
C、根据使用胶头滴管滴加少量液体的方法进行分析判断.
D、根据给试管中的液体加热的方法进行分析判断.
解答 解:A、闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,图中所示操作错误.
B、向试管中装块状固体药品时,先将试管横放,用镊子把块状固体放在试管口,再慢慢将试管竖立起来,图中所示操作错误.
C、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作正确.
D、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的$\frac{1}{3}$,图中所示操作正确.
故选:CD.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.把足量锌粒加入装有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体.在反应过程中,溶液的温度也先随之升高,最后下降到室温.于是,同学们设计实验来探究“一定质量的锌粒和同体积盐酸反应快慢的影响因素”.测得实验数据如下:
一定质量的锌粒与同体积盐酸溶液反应实验数据表
(1)锌粒和盐酸反应的化学化学方程式为Zn+2HCl═ZnCl2+H2↑.
(2)分析实验数据得出:一定质量的锌粒和同体积盐酸反应,影响锌和酸反应快慢的主要因素有盐酸溶液浓度、反应时溶液温度.
(3)可以通过比较反应开始到2分钟产生的气体体积(或相同时间内产生的气体体积)实验数据来确定锌和酸反应的快慢.
(4)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快原因金属锌和盐酸反应放出热量,加快反应速率.
一定质量的锌粒与同体积盐酸溶液反应实验数据表
| 盐酸溶液 浓度 | 反应开始时酸溶液的 温度 | 反应开始到2分钟产生的 气体体积 | 反应结束共产生 气体体积 |
| 5% | 20℃ | 10mL | 60mL |
| 10% | 20℃ | 19mL | 118mL |
| 15% | 20℃ | 28mL | 175mL |
| 5% | 35℃ | 28mL | 60mL |
| 10% | 35℃ | 72mL | 118mL |
| 15% | 35℃ | 103mL | 175mL |
(2)分析实验数据得出:一定质量的锌粒和同体积盐酸反应,影响锌和酸反应快慢的主要因素有盐酸溶液浓度、反应时溶液温度.
(3)可以通过比较反应开始到2分钟产生的气体体积(或相同时间内产生的气体体积)实验数据来确定锌和酸反应的快慢.
(4)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快原因金属锌和盐酸反应放出热量,加快反应速率.
11.物质的性质决定了物质的用途.下列几种常见物质的性质、用途不一致的是( )
| A. | 氮气的化学性质稳定,可用作保护气 | |
| B. | 酒精具有可燃性,可用作燃料 | |
| C. | 烧碱具有碱性,可用于除过多的胃酸 | |
| D. | 干冰易升华吸热,可用于人工降雨 |
8.在pH=11的溶液中能大量共存的离子是( )
| A. | Ba2+、Cl-、K+、NO3- | B. | Cu2+、SO42-、K+、NO3- | ||
| C. | Na+、Cl-、Mg2+、SO42- | D. | Na+、CO32-、NH4+、Cl-、 |
15.下列实验操作图示正确的是( )
| A. | 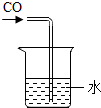 处理尾气 | B. |  盛放二氧化碳 | C. | 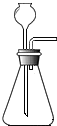 实验室制取CO2 | D. | 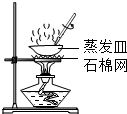 蒸发食盐水 |
9.材料是人类生存和发展的物质基础,下列物品的主要生产材质不是通过化学变化获取的是( )
| A. | 金缕衣 | B. | 马踏飞燕(青铜器) | C. | 少林剑(铁器) | D. | 陶瓷制品 |
10.交警用于检测司机是否酒后开车的检测仪中含有的一种成份是重铬酸钾(K2Cr2O7),其中铬元素的化合价是( )
| A. | +3 | B. | +6 | C. | +5 | D. | +4 |
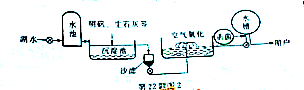
 水是我们接触最多的物质.
水是我们接触最多的物质.