题目内容
16.对物质进行分类学习是研究化学的重要方法.下列有关物质的分类错误的是( )| A. | 硝酸钾-盐 | B. | 硫酸-酸 | C. | 纯碱-碱 | D. | 氧化铁-氧化物 |
分析 根据酸是指在电离时产生的阳离子全部是氢离子的化合物;碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;盐是由金属离子(或铵根离子)和酸根离子组成的化合物;氧化物是指由两种元素组成且一种是氧元素的化合物;进行分析判断.
解答 解:A、硝酸钾是由钾离子和硝酸根离子组成的化合物,属于盐,故选项分类正确.
B、硫酸是由氢离子和硫酸根离子构成的化合物,属于酸,故选项分类正确.
C、纯碱是碳酸钠的俗称,是由钠离子和碳酸根离子组成的化合物,属于盐,故选项分类错误.
D、氧化铁是由铁元素和氧元素组成的化合物,属于氧化物,故选项分类正确.
故选:C.
点评 本题难度不大,考查物质类别的判别,抓住酸、碱、盐、氧化物的特征、熟悉常见的物质的组成是正确解答本题的关键.

练习册系列答案
相关题目
6.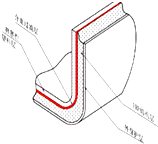 玻璃钢如图所示,可以代替钢材制造机器零件和汽车、船舶外壳等.它是以玻璃纤维及其制品(玻璃布、带、毡、纱等)作为增强材料,以合成树脂作基体材料,玻璃钢属于( )
玻璃钢如图所示,可以代替钢材制造机器零件和汽车、船舶外壳等.它是以玻璃纤维及其制品(玻璃布、带、毡、纱等)作为增强材料,以合成树脂作基体材料,玻璃钢属于( )
 玻璃钢如图所示,可以代替钢材制造机器零件和汽车、船舶外壳等.它是以玻璃纤维及其制品(玻璃布、带、毡、纱等)作为增强材料,以合成树脂作基体材料,玻璃钢属于( )
玻璃钢如图所示,可以代替钢材制造机器零件和汽车、船舶外壳等.它是以玻璃纤维及其制品(玻璃布、带、毡、纱等)作为增强材料,以合成树脂作基体材料,玻璃钢属于( )| A. | 金属材料 | B. | 合成材料 | C. | 复合材料 | D. | 无机非金属材料 |
7.海水蕴藏着丰富的化学资源,目前世界60%的镁是从海水中提取的.其主要流程如图所示.某校兴趣小组同学对从海水中提取金属镁的过程进行了有关探究.
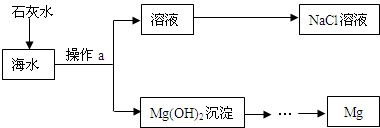
(1)在实验室进行操作a分离后的溶液(海水)中含有CaCl2等杂质,可向其中加入过量的Na2CO3(填化学式,后同)、适量的HCl,蒸发结晶,以除去CaCl2制得较为纯净的NaCl晶体.
(2)兴趣小组同学取一定量的海水样品,分别加入NaOH溶液,进行实验,测得的实验数据如表:
观察与分析上述数据,并计算
①海水样品中氯化镁的质量分数是多少?(计算结果精确到0.001%)
②若从1t这种海水中可提取多少千克金属镁?

(1)在实验室进行操作a分离后的溶液(海水)中含有CaCl2等杂质,可向其中加入过量的Na2CO3(填化学式,后同)、适量的HCl,蒸发结晶,以除去CaCl2制得较为纯净的NaCl晶体.
(2)兴趣小组同学取一定量的海水样品,分别加入NaOH溶液,进行实验,测得的实验数据如表:
| 实验1 | 实验2 | 实验3 | |
| 海水样品质量/g | 100 | 100 | 100 |
| 加入NaOH溶液质量/g | 10 | 15 | 20 |
| 生成沉淀物的质量/g | 0.22 | 0.29 | 0.29 |
①海水样品中氯化镁的质量分数是多少?(计算结果精确到0.001%)
②若从1t这种海水中可提取多少千克金属镁?
4.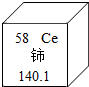 稀土元素是一类有重要用途的资源,铈是一种常见的稀土元素,下列说法中正确的( )
稀土元素是一类有重要用途的资源,铈是一种常见的稀土元素,下列说法中正确的( )
 稀土元素是一类有重要用途的资源,铈是一种常见的稀土元素,下列说法中正确的( )
稀土元素是一类有重要用途的资源,铈是一种常见的稀土元素,下列说法中正确的( )| A. | 铈属非金属元素 | B. | 铈的相对原子质量是140.1克 | ||
| C. | 铈原子的质子数为58 | D. | 铈原子中的中子数为58 |
11.下列生活中的变化,其中涉及化学变化的是( )
| A. | 玉石“变”手镯 | B. | 高粱“变”美酒 | ||
| C. | 树根“变”根雕 | D. | 玩具机器人“变”形 |
1.下列化学方程式书写正确的是( )
| A. | 镁条燃烧:Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | |
| B. | 双氧水中加入少量MnO2:H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2↑+O2↑ | |
| C. | 高炉炼铁:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | |
| D. | 烧碱溶液滴入硫酸铜溶液中:NaOH+CuSO4=NaSO4+Cu(OH)2↓ |
6.下列基本的实验操作正确的是( )
| A. |  测液体PH | B. |  干燥氨气 | C. |  检验CO2性质 | D. |  稀释浓硫酸 |