题目内容
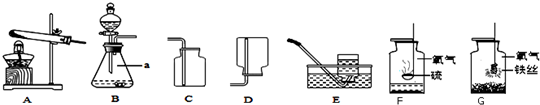
根据如图回答问题.
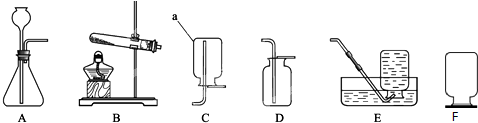
(1)仪器a的名称是 .
(2)实验室用高锰酸钾制取氧气的符号表达式为 ,选用的收集装置是 (填字母序号,下同).
(3)实验室用过氧化氢溶液中加入二氧化锰的方法制取氧气,选用的发生装置是 ,其中二氧化锰起 作用.
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,选用的发生装置是 .甲烷气体一般采用装置E进行收集,收集满后集气瓶的放置方式如图F所示,据此可推断甲烷一定具备的物理性质是 .

(1)仪器a的名称是
(2)实验室用高锰酸钾制取氧气的符号表达式为
(3)实验室用过氧化氢溶液中加入二氧化锰的方法制取氧气,选用的发生装置是
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,选用的发生装置是
考点:氧气的制取装置,氧气的收集方法,催化剂的特点与催化作用,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)熟悉常见仪器;
(2)高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气;气体发生装置取决于反应物的状态和反应条件;
(3)二氧化锰能加快过氧化氢的分解速率;根据氧气的性质来选择收集方法.
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,因此需要加热;甲烷气体一般采用装置D进行收集,收集满后集气瓶的放置方式如图F所示,因此甲烷有难溶于水,密度比空气的密度小的性质.
(2)高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气;气体发生装置取决于反应物的状态和反应条件;
(3)二氧化锰能加快过氧化氢的分解速率;根据氧气的性质来选择收集方法.
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,因此需要加热;甲烷气体一般采用装置D进行收集,收集满后集气瓶的放置方式如图F所示,因此甲烷有难溶于水,密度比空气的密度小的性质.
解答:解:(1)仪器a是集气瓶;
(2)高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑;因为氧气不易溶于水,且密度比空气大,故可用排水法或向上排空气法来收集氧气.
(3)在反应中,二氧化锰加快了过氧化氢的分解速率,而本身的质量和化学性质均不改变,充当反应的催化剂,起到了催化作用;因为反应物是固体与液体,反应不需要加热,故选择A来制取氧气;
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,因此需要加热;甲烷气体一般采用装置D进行收集,收集满后集气瓶的放置方式如图F所示,因此甲烷有难溶于水,密度比空气的密度小的性质;
故答案为:(1)集气瓶;(2)2KMnO4
K2MnO4+MnO2+O2↑;D或E;(3)A;催化.(4)B;难溶于水;密度比空气的密度小;
(2)高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4
| ||
(3)在反应中,二氧化锰加快了过氧化氢的分解速率,而本身的质量和化学性质均不改变,充当反应的催化剂,起到了催化作用;因为反应物是固体与液体,反应不需要加热,故选择A来制取氧气;
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,因此需要加热;甲烷气体一般采用装置D进行收集,收集满后集气瓶的放置方式如图F所示,因此甲烷有难溶于水,密度比空气的密度小的性质;
故答案为:(1)集气瓶;(2)2KMnO4
| ||
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和验满方法等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
下列变化中,既属于化合反应,也属于氧化反应的是( )
| A、硫在氧气中燃烧 |
| B、石蜡在空气中燃烧 |
| C、高锰酸钾受热分解 |
| D、过氧化氢分解 |
在研究质量守恒定律时,将镁条在空气中点燃,待反应完毕后称量,发现燃烧后留下的固体物质质量比镁条的质量大,该实验最终解释合理的是( )
| A、一部分镁条可能与空气中别的物质反应生成固体粉末 |
| B、没有在封闭环境中做实验 |
| C、镁条在燃烧过程中由于温度较高,部分生成物呈气态逸进空气中 |
| D、符合质量守恒定律 |
下列反应属于分解反应的是( )
A、4P+5O2
| ||||
B、2H2O
| ||||
C、C+2CuO
| ||||
| D、HCl+NaOH═NaCl+H2O |
 如图所示分别向试管中加入下列物质,能使U形管左侧液面显著升高的是( )
如图所示分别向试管中加入下列物质,能使U形管左侧液面显著升高的是( )| A、食盐 |
| B、浓硫酸 |
| C、NH4NO3固体 |
| D、NaOH固体 |