题目内容
某校化学兴趣小组的同学根据实验室提供的仪器和药品,在老师的指导下从如图中选择装置进行了氧气的制备实验.
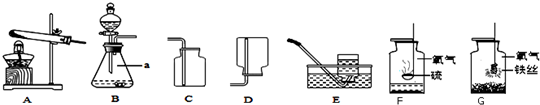
(1)写出仪器a的名称: .
(2)甲同学用过氧化氢溶液和二氧化锰制取氧气,反应的符号表达式为: .制取和收集氧气可选用的装置是 ;用实验装置E收集某气体,其中水的作用是 ;实验装置F的集气瓶中预先加入了少量水,其作用是 .通过F、G两个实验,结合课堂学习,你认为在“集气瓶中进行燃烧的实验”应该注意的问题是 .
(3)乙同学称取一定质量的高锰酸钾固体放入大试管中,将温度控制在250℃加热制取氧气.实验结束时,乙同学发现用排水法收集到的氧气大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的二氧化锰分解放出氧气;
猜想Ⅱ:反应生成的锰酸钾分解放出氧气
猜想Ⅲ:反应生成的锰酸钾和二氧化锰分解都放出氧气.
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的二氧化锰固体于试管中,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,则猜想 错误;第二组同学取锰酸钾固体于试管中在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是 .
【拓展延伸】实验发现,氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾分解速率大大加快.请说明高锰酸钾在氯酸钾的分解反应中是否作催化剂,为什么? .

(1)写出仪器a的名称:
(2)甲同学用过氧化氢溶液和二氧化锰制取氧气,反应的符号表达式为:
(3)乙同学称取一定质量的高锰酸钾固体放入大试管中,将温度控制在250℃加热制取氧气.实验结束时,乙同学发现用排水法收集到的氧气大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的二氧化锰分解放出氧气;
猜想Ⅱ:反应生成的锰酸钾分解放出氧气
猜想Ⅲ:反应生成的锰酸钾和二氧化锰分解都放出氧气.
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的二氧化锰固体于试管中,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,则猜想
【拓展延伸】实验发现,氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾分解速率大大加快.请说明高锰酸钾在氯酸钾的分解反应中是否作催化剂,为什么?
考点:氧气的制取装置,氧气的化学性质,氧气的收集方法,催化剂的特点与催化作用,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)熟悉常用仪器的名称和用途;
(2)根据用过氧化氢溶液和二氧化锰制取氧气反应,写出反应的文字表达式,根据反应的特点分析反应的类型,根据氧气的性质分析收集可选用的装置.
(3)根据催化剂的性质及氧气的性质分析回答.
(2)根据用过氧化氢溶液和二氧化锰制取氧气反应,写出反应的文字表达式,根据反应的特点分析反应的类型,根据氧气的性质分析收集可选用的装置.
(3)根据催化剂的性质及氧气的性质分析回答.
解答:解:(1)由装置可知.标号仪器a的名称锥形瓶;
(2)用过氧化氢溶液和二氧化锰制取氧气,反应的表达式为:2H2O2
2H2O+O2↑,根据反应物为固体和液体,反应条件不许加热.由于氧气不易溶于水,密度比空气略大,所以,制取和收集氧气可选用的装置是BC或BE.用实验装置E收集某气体,其中水的作用是排进空气;实验装置F的集气瓶中预先加入了少量水,其作用是防止生成物炸裂集气瓶;
通过以上F、G实验分析可知在“集气瓶中进行燃烧的实验”要注意环境保护,并注意仪器安全;
(3)【实验验证】第一组同学加热二氧化锰一段时间,由二氧化锰的质量不变可知,反应生成的二氧化锰不能分解放出氧气;由于氧气有助燃性,所以,该组同学选择的实验方法是:将带火星的木条放在集气瓶口,木条复燃,证明猜想Ⅱ正确.
【拓展延伸】氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾分解速率大大加快. 高锰酸钾不是催化剂.因为高锰酸钾在反应后的质量和性质发生了变化.
故答为:(1)锥形瓶;(2)2H2O2
2H2O+O2↑;BC或BE;排尽空气;防止生成物炸裂集气瓶;注意环境保护、注意安全.
(3)【实验验证】Ⅰ;将带火星的木条放在集气瓶口,木条复燃,证明猜想Ⅱ正确.【拓展延伸】高锰酸钾不是催化剂.因为高锰酸钾在反应后的质量和性质发生了变化.
(2)用过氧化氢溶液和二氧化锰制取氧气,反应的表达式为:2H2O2
| ||
通过以上F、G实验分析可知在“集气瓶中进行燃烧的实验”要注意环境保护,并注意仪器安全;
(3)【实验验证】第一组同学加热二氧化锰一段时间,由二氧化锰的质量不变可知,反应生成的二氧化锰不能分解放出氧气;由于氧气有助燃性,所以,该组同学选择的实验方法是:将带火星的木条放在集气瓶口,木条复燃,证明猜想Ⅱ正确.
【拓展延伸】氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾分解速率大大加快. 高锰酸钾不是催化剂.因为高锰酸钾在反应后的质量和性质发生了变化.
故答为:(1)锥形瓶;(2)2H2O2
| ||
(3)【实验验证】Ⅰ;将带火星的木条放在集气瓶口,木条复燃,证明猜想Ⅱ正确.【拓展延伸】高锰酸钾不是催化剂.因为高锰酸钾在反应后的质量和性质发生了变化.
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和过滤的仪器等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
物质发生化学变化时一定会发生改变的是( )
| A、分子种类 | B、原子种类 |
| C、元素种类 | D、分子数目 |
 随着日本福岛核电站放射性碘泄漏,碘这种元素被人们所认知.如图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图.下列说法错误的是( )
随着日本福岛核电站放射性碘泄漏,碘这种元素被人们所认知.如图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图.下列说法错误的是( )| A、碘的相对原子质量为126.9,原子核内质子数为53 |
| B、碘原子最外层有7个电子,与氯原子的化学性质相似 |
| C、碘盐中含有碘酸钾(KIO3),KIO3中碘元素的化合价为-1 |
| D、碘元素属于非金属元素,碘原子在化学反应中容易得到电子 |
下列有关实验室用过氧化氢制氧气的叙述中,正确的是( )
| A、过氧化氢受热后,也不放出氧气 |
| B、要使受热分解放出氧气,必须加入二氧化锰 |
| C、二氧化锰在化学反应前后质量和化学性质都保持不变 |
| D、二氧化锰是一切化学反应的催化剂 |
有关 2H2O
2H2↑+O2↑的读法,正确的是( )
| ||
| A、水等于氢气加氧气 |
| B、水在通电的条件下,生成氢气加氧气 |
| C、2份水反应生成2份氢气和1份二氧气 |
| D、每36份质量的水生成32份质量的氧气和4份质量的氢气 |
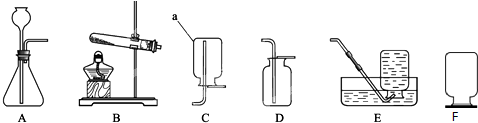
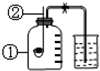 气密性良好的实验装置(如图所示)中仪器①、②的名称分别是
气密性良好的实验装置(如图所示)中仪器①、②的名称分别是