题目内容
5.我国化工专家侯德榜先生改进西方的制碱技术,成功发明了联合制碱法(又称侯氏制碱法),为纯碱和氮肥工业技术的发展作出了杰出的贡献.(1)侯氏制碱法中的碱是指Na2CO3(写化学式).
(2)反应分两步,第一步向氨饱和的食盐水中通入足量CO2,发生如下反应:NaCl+CO2+NH3+H2O=NaHCO3+X,则X是NH4Cl.
(3)纯碱的用途十分广泛.写出用纯碱制备烧碱的一个反应方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
分析 (1)侯氏制碱法中的碱是指碳酸钠,写出其化学式即可.
(2)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
(3)纯碱与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,写出反应的化学方程式即可.
解答 解:(1)侯氏制碱法中的碱是指碳酸钠,其化学式为:Na2CO3.
(2)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式NaCl+CO2+NH3+H2O=NaHCO3+X,反应前钠、氯、碳、氧、氮、氢原子个数分别为1、1、1、3、1、5,反应后的生成物中钠、氯、碳、氧、氮、氢原子个数分别为1、0、1、3、0、1,根据反应前后原子种类、数目不变,则每个X分子由1个氮原子、4个氢原子和1个氯原子构成,则物质X的化学式为NH4Cl.
(3)纯碱与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
故答案为:(1)Na2CO3;(2)NH4Cl;(3)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 本题难度不大,掌握侯氏制碱法的碱是指碳酸钠、化学反应前后原子守恒、盐的化学性质、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.2g氢气和2g氧气在点燃条件下充分反应,能生成水( )
| A. | 18 g | B. | 4.5 g | C. | 2.25 g | D. | 36 g |
13.蓬溪县高平镇盛产茶叶,茶叶中含茶氨酸(化学式为C7H14O3N2)、锌、硒等多种成分,茶树适宜在pH为5~6的土壤中生长.下列说法不正确的是( )
| A. | 茶氨酸属于混合物,锌、硒指单质 | |
| B. | 一个茶氨酸分子中含3个氧原子 | |
| C. | 茶氨酸由碳、氢、氧、氮四种元素组成 | |
| D. | 茶树不宜在碱性土壤中生长 |
17.化学反应有不同的分类方法.关于下列反应说法正确的是( )
(1)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 (2)CO+CuO$\frac{\underline{\;加热\;}}{\;}$CO2+Cu (3)NaOH+HCl=NaCl+H2O
(4)H2O+CO2=H2CO3 (5)CO2+2NaOH═Na2CO3+H2O (6)Zn+H2SO4═ZnSO4+H2↑
(1)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 (2)CO+CuO$\frac{\underline{\;加热\;}}{\;}$CO2+Cu (3)NaOH+HCl=NaCl+H2O
(4)H2O+CO2=H2CO3 (5)CO2+2NaOH═Na2CO3+H2O (6)Zn+H2SO4═ZnSO4+H2↑
| A. | (2)、(4)属于分解反应 | B. | (2)、(6)属于置换反应 | ||
| C. | (3)、(5)属于复分解反应 | D. | (1)、(4)属于化合反应 |
15.下列物质转化不能一步实现的是( )
| A. | C--CO | B. | CO--CO2 | C. | CaCO3--CO2 | D. | KNO3--KCl |

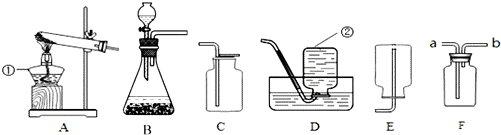
 如图是实验室制备制取氧气的常用装置.
如图是实验室制备制取氧气的常用装置.