题目内容
5.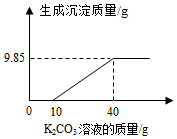 做实验时,小科取了40mL的Ba(OH)2溶液,并随手倒入等量的稀盐酸(均未知浓度).老师发现后,递给他一瓶未知质量分数的K2CO3溶液,让小科来检测混合溶液的酸碱性.小科在混合液中慢慢滴入K2CO3,溶液,获得相关数据并绘成如图所示图象.
做实验时,小科取了40mL的Ba(OH)2溶液,并随手倒入等量的稀盐酸(均未知浓度).老师发现后,递给他一瓶未知质量分数的K2CO3溶液,让小科来检测混合溶液的酸碱性.小科在混合液中慢慢滴入K2CO3,溶液,获得相关数据并绘成如图所示图象.(1)刚加入K2CO3溶液时,发现没有沉淀生成,却有气泡产生,则原混合溶液呈酸性 (填“酸性”、“碱性”或“中性”),其中所含的溶质有BaCl2、HCl(用化学式表示);
(2)计算K2CO3溶液中溶质的质量分数.(BaCl2+K2CO3=BaCO3↓+2KCl)
分析 氢氧化钡和稀盐酸反应生成氯化钡和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和氯化钡反应生成碳酸钡沉淀和氯化钠,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)刚加入K2CO3溶液时,发现没有沉淀生成,却有气泡产生,说明稀盐酸过量,则原混合溶液呈酸性,其中所含的溶质有BaCl2、HCl.
故填:酸性;BaCl2、HCl.
(2)设30g碳酸钾溶液中碳酸钾质量为x,
BaCl2+K2CO3=BaCO3↓+2KCl,
138 197
x 9.85g
$\frac{138}{x}$=$\frac{197}{9.85g}$,
x=6.9g,
K2CO3溶液中溶质的质量分数为:$\frac{6.9g}{30g}$×100%=23%,
答:K2CO3溶液中溶质的质量分数为23%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.某同学把24.5g的KClO3和7.5g的MnO2混合物放在试管中,经加热完全反应并冷却后,称得试管中残余物质量为22.4g.则下列数据分析正确的是( )
| A. | 反应中产生的氧气质量为2.1g | B. | 22.4g的残余物中含有7.5gMnO2 | ||
| C. | 22.4g残余物是氯化钾 | D. | 反应中产生的氧气质量为9.6g |
20.三甲基一氯硅[(CH3)3SiCl]是一种生产有机硅化合物的原料,遇火能燃烧甚至会发生爆炸,与水接触可产生盐酸.则下列说法错误的是( )
| A. | 保存三甲基一氯硅时应密封防水 | |
| B. | 三甲基一氯硅充分燃烧的产物之一是二氧化碳 | |
| C. | 三甲基一氯硅水溶液的pH小于7 | |
| D. | 三甲基一氯硅不是有机物 |
10.将某无色混合气体依次进行如下实验(假设每步实验均作用完全):①通过氢氧化钠固体后,气体体积变小;②通过灼热的氧化铜粉末,粉末变为红色;③通过白色硫酸铜粉末,粉末变为蓝色;④通过澄清石灰水,溶液变浑浊.试推断原混合气体的组成可能是( )
| A. | H2、CO | B. | CO、CO2、H2O(气) | C. | H2、CO2 | D. | H2、CO、H2O(气) |