题目内容
10.将某无色混合气体依次进行如下实验(假设每步实验均作用完全):①通过氢氧化钠固体后,气体体积变小;②通过灼热的氧化铜粉末,粉末变为红色;③通过白色硫酸铜粉末,粉末变为蓝色;④通过澄清石灰水,溶液变浑浊.试推断原混合气体的组成可能是( )| A. | H2、CO | B. | CO、CO2、H2O(气) | C. | H2、CO2 | D. | H2、CO、H2O(气) |
分析 根据各种气体的性质和各操作的目的分析,氢氧化钠固体能吸收水和二氧化碳,灼热的氧化铜能和具有还原性的气体反应,白色硫酸铜粉末遇到水会变蓝色,二氧化碳能使澄清的石灰水变浑浊.
解答 解:①通过氢氧化钠固体后,气体体积变小;氢氧化钠固体吸收水和二氧化碳,体积会减小,这证明混合气体中至少含有CO2、H2O(气)中的一种,而且通过氢氧化钠固体后全部吸收;
②通过赤热的氧化铜时,固体变为红色;可能有CO还原氧化铜,也可能是氢气还原氧化铜,也可能是两者都有;
③通过白色硫酸铜粉末时,粉末变为蓝色,证明有水生成,而这部分水来源于氢气还原氧化铜时生成,所以必须有氢气;
④通过澄清石灰水时,溶液变浑浊证明有二氧化碳,而二氧化碳来源于一氧化碳还原氧化铜,所以必须有一氧化碳.
综上分析:混合气体中定含有CO、H2,至少含有H2O、CO2中的一种.
故选D.
点评 本题考查混合气体的推断,题目难度不大,抓住题中反应的典型现象,掌握元素化合物的性质是做好此类题目的关键.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
20.小亮在室温20℃做食盐溶解实验时,列出了以下一组数据,下列叙述正确的是( )
| 实验序号 | 水的质量/g | 所加NaCl的质量/g | 所得溶液的质量/g |
| ① | 100 | 20 | 120 |
| ② | 100 | 30 | 130 |
| ③ | 100 | 40 | 136 |
| ④ | 100 | 50 | 136 |
| A. | ①②所得溶液是20℃时NaCl的饱和溶液 | |
| B. | 20℃时,NaCl的溶解度为36g | |
| C. | ①②③所得溶液是20℃时NaCl的不饱和溶液 | |
| D. | ①所得溶液的溶质质量分数为20% |
2.用托盘天平称量一未知质量的烧杯.现用“↓”表示向托盘上增加砝码,用“↑”表示从托盘上减少砝码.请用“↑”和“↓”在表中表示你的称量过程,并在下图中用“Ⅰ”表示游码在标尺上的位置(若烧杯的实际质量为37.6g).
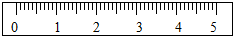

| 砝码/g | 50 | 20 | 20 | 10 | 5 |
| 取用情况 |
19.在科学学习中,经常对科学实验现象的观察和分析总结,有助于加深对科学知识的理解并学会科学探究的方法.下列对实验现象的分析合理的是( )
| A. | 向某无色溶液中滴入硫酸试液,产生白色沉淀,证明该溶液是氯化钡溶液 | |
| B. | 向某无色溶液中滴入硫酸铜溶液,产生蓝色沉淀,证明该溶液是氢氧化钠 | |
| C. | 某白色固体与熟石灰混合后加热,产生可使湿润红色石蕊试纸变蓝色的气体,证明该白色固体是铵盐 | |
| D. | 把燃着的木条伸入某无色气体的集气瓶中,火焰熄灭,证明该气体是二氧化碳 |
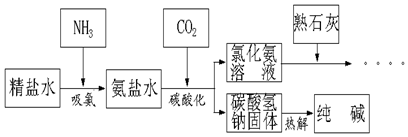
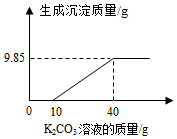 做实验时,小科取了40mL的Ba(OH)2溶液,并随手倒入等量的稀盐酸(均未知浓度).老师发现后,递给他一瓶未知质量分数的K2CO3溶液,让小科来检测混合溶液的酸碱性.小科在混合液中慢慢滴入K2CO3,溶液,获得相关数据并绘成如图所示图象.
做实验时,小科取了40mL的Ba(OH)2溶液,并随手倒入等量的稀盐酸(均未知浓度).老师发现后,递给他一瓶未知质量分数的K2CO3溶液,让小科来检测混合溶液的酸碱性.小科在混合液中慢慢滴入K2CO3,溶液,获得相关数据并绘成如图所示图象.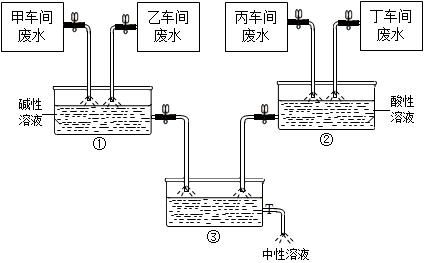 合理化处理废水是当前防治废水中的有害或有毒物质对环境造成污染的重要举措.某化学试剂厂甲、乙、丙、丁四个车间排放的废水中,主要成分分别含有CuCl2、HCl、Na2CO3、NaOH的一种.甲车间的废水呈蓝色.通过调节废水流量,使乙、丁两个车间废水相对过量,最终排出的废水呈中性.处理过程如图所示,在第①反应池中出现大量的蓝色沉淀,在第②反应池中出现大量的气泡.请回答:
合理化处理废水是当前防治废水中的有害或有毒物质对环境造成污染的重要举措.某化学试剂厂甲、乙、丙、丁四个车间排放的废水中,主要成分分别含有CuCl2、HCl、Na2CO3、NaOH的一种.甲车间的废水呈蓝色.通过调节废水流量,使乙、丁两个车间废水相对过量,最终排出的废水呈中性.处理过程如图所示,在第①反应池中出现大量的蓝色沉淀,在第②反应池中出现大量的气泡.请回答: