题目内容
19.如图所示为实验室中常见的气体制备和收集装置.请回答下列问题:
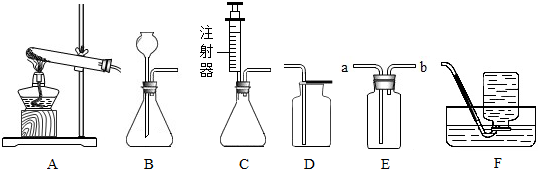
(1)实验室用高锰酸钾制取氧气时,应选用发生装置A(填序号),反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑此反应类型是分解反应;若用装置D收集氧气,验满的方法是将带火星的木条放在集气瓶口,木条复燃,证明集满了氧气.
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是控制氧气产生的快慢和量的多少.欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从b(填“a”或“b”)端通入;
(3)实验室检验二氧化碳的方法是(用化学方程式表示)Ca(OH)2+CO2=CaCO3↓+H2O.欲使用装置E用排空气法收集二氧化碳,则气体应从a(填“a”或“b”)端通入;一般不用F装置收集CO2的原因是二氧化碳能溶于水.
(4)已知一氧化氮气体难溶于水,在空气中最容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置F(填序号)
分析 (1)根据方程式的书写方法、发生装置的选择方法、氧气的验满方法来分析;
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,该装置的优点是:控制氧气产生的快慢和量的多少;氧气的密度比水小;
(3)根据二氧化碳的性质分析解答;
(4)根据一氧化氮的性质分析收集的方法及装置.
解答 解:(1)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应符合“一变多”的特征,属于分解反应.是由固体加热制氧气,所以选择装置A来制取;D装置收集氧气时,验满的方法是将带火星的木条放在集气瓶口,木条复燃,证明集满了氧气.
故答案为:A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;分解;将带火星的木条放在集气瓶口,木条复燃,证明集满了氧气;
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,该装置的优点是:控制氧气产生的快慢和量的多少;欲使用装置E用排水法收集氧气,先将瓶中装满水,因为气体的密度总比水的密度小,因此再将气体从b进入即可,故答案为:控制氧气产生的快慢和量的多少;b;
(3)二氧化碳能使澄清的石灰水变浑浊,所以常用澄清的石灰水来检验二氧化碳气体,二氧化碳的密度比空气大,所以用装置E收集二氧化碳时,二氧化碳从长管进入,二氧化碳能溶于水,所以一般不用排水法收集二氧化碳;故填:Ca(OH)2+CO2=CaCO3↓+H2O;a;二氧化碳能溶于水;
(4)由于一氧化氮气体难溶于水,在空气中容易与氧气发生反应,只能用排水法收集,收集装置是:F.故填:F.
点评 本考点主要考查气体的制取装置和收集装置的选择,同时也考查了改进装置的优点等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 成人体内约含钙1.2kg,其中99%存在于骨骼和牙齿中.在元素周期表中,钙元素的信息如图所示.下列说法不正确的是( )
成人体内约含钙1.2kg,其中99%存在于骨骼和牙齿中.在元素周期表中,钙元素的信息如图所示.下列说法不正确的是( )| A. | 钙原子的核外电子数为20 | B. | 钙元素属于金属元素 | ||
| C. | 钙元素在地壳中的含量为40.08% | D. | 钙元素的原子序数为20 |
(1)根据表中提供的信息,填写有关“碳”物质对应的信息
| 物质用途 | 金刚石切割玻璃 | 石墨做电极 | 活性炭净水 |
| 对应性质 | ① | ② | ③ |
(3)液态二氧化碳灭火器可用于扑救档案资料室发生的火灾,下列说法正确的有AB(填序号).
A.液态二氧化碳气化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳汽化时吸热,降低了可燃物的着火点
(4)二氧化碳是一种宝贵的资源.固定和利用二氧化碳的一个成功范例是:在高温高压下CO2和NH3可以合成尿素【化学式:CO(NH2)2】,同时生成水,写出该反应的化学反应方程式CO2+2NH3$\frac{\underline{\;高温高压\;}}{\;}$CO(NH2)2+H2O.
| A. | 排水法收集氧气时,当导管口一有气泡冒出就立即收集 | |
| B. | 稀释浓硫酸时,沿烧杯壁将水缓缓注入盛有浓硫酸的烧杯中,并用玻璃棒不断搅拌 | |
| C. | 过滤时,将玻璃棒斜靠在单层滤纸的一边 | |
| D. | 加热试管中的液体时,先使试管底部均匀受热,后用酒精灯的灯焰固定加热 |
| A. | Na2CO3 | B. | CO2 | C. | NaOH | D. | H2SO4 |
 将一张滤纸剪成四等份,用铜片、锌片、发光二极管、导线在玻璃片上连接成如图所示的装置,在四张滤纸上滴入稀H2SO4直至全部湿润.下列叙述不正确的是( )
将一张滤纸剪成四等份,用铜片、锌片、发光二极管、导线在玻璃片上连接成如图所示的装置,在四张滤纸上滴入稀H2SO4直至全部湿润.下列叙述不正确的是( )| A. | 锌片上有气泡,铜片溶解 | |
| B. | 若用碳棒代替铜,也会产生同样的现象 | |
| C. | 如果将稀硫酸换成柠檬汁,二极管也会发光 | |
| D. | 该装置至少有两种形式的能量转换 |


 小明同学为探究二氧化碳的性质,设计了下列实验.
小明同学为探究二氧化碳的性质,设计了下列实验.