题目内容
7.下列实验操作正确的是( )| A. | 排水法收集氧气时,当导管口一有气泡冒出就立即收集 | |
| B. | 稀释浓硫酸时,沿烧杯壁将水缓缓注入盛有浓硫酸的烧杯中,并用玻璃棒不断搅拌 | |
| C. | 过滤时,将玻璃棒斜靠在单层滤纸的一边 | |
| D. | 加热试管中的液体时,先使试管底部均匀受热,后用酒精灯的灯焰固定加热 |
分析 A、根据用排水法收集氧气的注意事项,进行分析判断.
B、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
C、过滤液体时,注意“一贴、二低、三靠”的原则.
D、根据加热试管中的液体时的注意事项,进行分析判断.
解答 解:A、排水法收集氧气时,当导管口一有气泡冒出不能立即收集,因为刚开始排出的气体是空气,故选项说法错误.
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;故选项说法错误.
C、过滤时,将玻璃棒斜靠在三层滤纸的一边,故选项说法错误.
D、加热试管中的液体时,先使试管底部均匀受热,后用酒精灯的灯焰固定加热,故选项说法正确.
故选:D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
18.某化学兴趣小组的同学用一瓶已经过滤的澄淸透明海水为原料,在实验室中模拟“侯氏制碱法”的制碱过程.
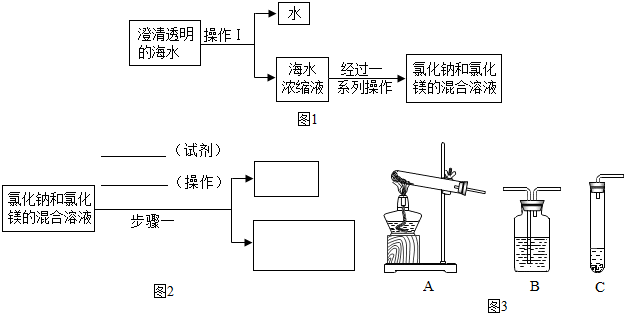
(1)从海水中分别得到纯净的水和氯化钠固体(其流程如图1),其中,操作I的名称是蒸发;完成这一操作实验,除了胶塞、导管、收集容器和铁架台外,还需要的主要仪器之一是酒精灯(只要求写出其中一种仪器名称).
(2)请完成实验设计思路图(图2),目的是从氯化钠和氯化镁的混合溶液中除去氯化镁,得到较纯净的氯化钠固体.(要求:①在图2箭头上/下方写出相应的试剂和实验操作;②在方框内写出相应的化学式;③可根据需要,仿照步骤1的写法将此图延伸.)
(3)已知有四种物质在30℃时的溶解度如表所示:
请根据溶解度表所提供的信息,用这四种物质分别作为反应物和生成物,写出一道复分解反应的化 学方程式.
NaCl+NH4HCO3=NaHCO3↓+NH4Cl.
“侯氏制碱法”既是向饱和氯化钠溶液中先后通入氨气〔NH4)和二氧化碳(CO2),使溶液中发生上述反应.
同学们利用图3装置B完成这一反应后,取其中的一种生成物,再利用装置A进行加热分解就得到了最后的产品Na2CO3(填化学式).

(1)从海水中分别得到纯净的水和氯化钠固体(其流程如图1),其中,操作I的名称是蒸发;完成这一操作实验,除了胶塞、导管、收集容器和铁架台外,还需要的主要仪器之一是酒精灯(只要求写出其中一种仪器名称).
(2)请完成实验设计思路图(图2),目的是从氯化钠和氯化镁的混合溶液中除去氯化镁,得到较纯净的氯化钠固体.(要求:①在图2箭头上/下方写出相应的试剂和实验操作;②在方框内写出相应的化学式;③可根据需要,仿照步骤1的写法将此图延伸.)
(3)已知有四种物质在30℃时的溶解度如表所示:
| 温度 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 30℃ | 36.3g | 27.0g | 11.1g | 41.1g |
NaCl+NH4HCO3=NaHCO3↓+NH4Cl.
“侯氏制碱法”既是向饱和氯化钠溶液中先后通入氨气〔NH4)和二氧化碳(CO2),使溶液中发生上述反应.
同学们利用图3装置B完成这一反应后,取其中的一种生成物,再利用装置A进行加热分解就得到了最后的产品Na2CO3(填化学式).
2.下列说法正确的是( )
| A. | 铝比铁的抗腐蚀性能强,故铝比铁的化学性质稳定 | |
| B. | 中和反应一定生成盐和水,但生成盐和水的反应不一定是中和反应 | |
| C. | 燃烧一般都伴随发光和放热现象,所以有发光和放热现象的变化都是燃烧 | |
| D. | 原子不显电性,所以构成原子的粒子也不显电性 |
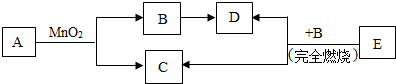 已知A、B、C、D、E五种物质之间存在以下的转化关系,其中A、C两种物质的组成元素相同,且常温下为液体.
已知A、B、C、D、E五种物质之间存在以下的转化关系,其中A、C两种物质的组成元素相同,且常温下为液体.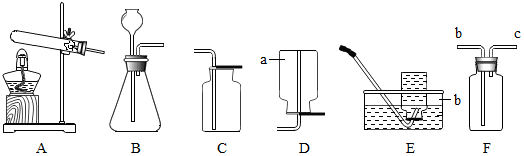
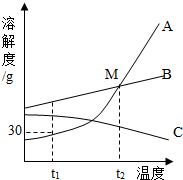 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: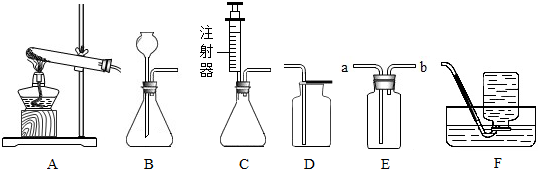
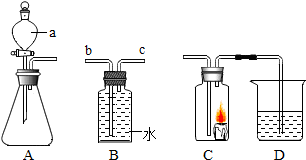 根据如图所示装置回答有关问题:
根据如图所示装置回答有关问题: