题目内容
9.根据下列装置,结合所学化学知识回答下列问题:
(1)写出图中标号仪器的名称:①长颈漏斗;
(2)实验室制取二氧化碳时,如需要随时控制反应速率并节约药品,发生装置最好选用B(填字母序号),其反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)在实验室里,可用硫化亚铁固体和稀硫酸的反应来制取硫化氢气体,在通常情况下硫化氢是一种无色、有臭鸡蛋气味的有毒气体,能溶于水且水溶液呈酸性,密度比空气的大,实验室制取硫化氢气体时应选用的收集装置是E(填字母序号),实验结束后剩余的硫化氢气体应该用氢氧化钠溶液来吸收以免污染空气.
分析 (1)熟悉常用化学仪器,了解它们的名称及用途;
(2)根据反应物的状态和反应条件选择发生装置和气体的收集方法选择的依据;
(3)据制取硫化氢的反应原理分析发生装置,并据硫化氢的密度和溶解性选择收集装置.结合硫化氢气体的性质解答.
解答 解:(1)由图知①是长颈漏斗;
(2)制取二氧化碳选用石灰石和稀盐酸常温下反应所以选用固液混合不加热装置,制取少量的选用试管不用锥形瓶,故实验室制取二氧化碳时,如需要随时控制反应速率并节约药品,发生装置最好选用B
;实验室制取CO2的反应原理是大理石(或石灰石)与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)实验室用硫化亚铁固体跟稀硫酸反应制取硫化氢气体,属于固液在常温下反应制取气体,发生装置应选用A;硫化氢气体密度比空气大,能溶于水,因此收集装置应选用E;由于硫化氢气体能溶于水且水溶液呈酸性,故可以用氢氧化钠溶液等碱性溶液吸收剩余的硫化氢气体.
故答案为:
(1)长颈漏斗;(2)B,CaCO3+2HCl═CaCl2+H2O+CO2↑.(3)E,氢氧化钠.
点评 本题考查了氧气及二氧化碳的制取、检验、验满等的基础知识,可以根据已有的知识解决.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
19.做氢气还原氧化铜实验,一段时间后停止加热,测得剩余固体中铜元素与氧元素的质量之比为8:1,则已反应的氧化铜与原氧化铜的质量比是( )
| A. | 1:2 | B. | 1:1 | C. | 32:1 | D. | 4:1 |
20.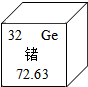 锗是重要的半导体材料,锗元素的相关信息如图,下列有关锗的说法正确的是( )
锗是重要的半导体材料,锗元素的相关信息如图,下列有关锗的说法正确的是( )
 锗是重要的半导体材料,锗元素的相关信息如图,下列有关锗的说法正确的是( )
锗是重要的半导体材料,锗元素的相关信息如图,下列有关锗的说法正确的是( )| A. | 属于非金属元素 | B. | 核电荷数为32 | ||
| C. | 原子序数为40 | D. | 相对原子质量为72.63g |
17.硬水会给我们的生活和生产带来许多麻烦,下列单一操作相对净化程度最高的是( )
| A. | 蒸馏 | B. | 煮沸 | C. | 沉淀 | D. | 过滤 |
18. 同学们发现将NaOH溶液和稀盐酸混合后没有明显现象,为了证明NaOH能与HCl发生中和反应,设计了如下实验:
同学们发现将NaOH溶液和稀盐酸混合后没有明显现象,为了证明NaOH能与HCl发生中和反应,设计了如下实验:
【解释与结论】写出NaOH与HCl反应的化学方程式NaOH+HCl═NaCl+H2O.
【反思与评价】同学们对实验2反应后所得溶液的酸碱性进行讨论,小玲同学认为呈碱性,小生同学认为呈中性,小柏同学认为也可能呈酸性,最后同学们否定了小玲同学的说法,其理由是红色逐渐消失;欲进一步确定实验2反应后所得溶液的酸碱性,其操作是用试管取少量所得溶液,滴入1-2滴紫色石蕊试液,振荡.
 同学们发现将NaOH溶液和稀盐酸混合后没有明显现象,为了证明NaOH能与HCl发生中和反应,设计了如下实验:
同学们发现将NaOH溶液和稀盐酸混合后没有明显现象,为了证明NaOH能与HCl发生中和反应,设计了如下实验:| 实验步骤 | 现象 | 结论 |
| 实验1.取少量NaOH溶液于试管中,向其中滴加几滴无色酚酞试液,振荡. | 溶液呈红色 | |
| 实验2.向实验1的试管中加入适量的稀盐酸,振荡. | 红色逐渐消失. | NaOH与HCl能反应. |
【反思与评价】同学们对实验2反应后所得溶液的酸碱性进行讨论,小玲同学认为呈碱性,小生同学认为呈中性,小柏同学认为也可能呈酸性,最后同学们否定了小玲同学的说法,其理由是红色逐渐消失;欲进一步确定实验2反应后所得溶液的酸碱性,其操作是用试管取少量所得溶液,滴入1-2滴紫色石蕊试液,振荡.

