题目内容
有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应).现取8g石灰石样品与足量的50g稀盐酸完全反应后,称得容器内的物质总质量为55.36g.
试回答下列问题:
(1)反应后容器内的物质有______.
(2)反应产生二氧化碳的质量为______.
(3)该石灰石样品中碳酸钙的质量分数是多少?
解:(1)由于石灰石样品中碳酸钙能与盐酸反应生成氯化钙水和二氧化碳,而烧杯中还含有不反应的二氧化硅以及剩余的盐酸,所以反应后容器内的物质有:SiO2、CaCl2、HCl、H2O;
(2)由质量守恒定律可知该反应生成的二氧化碳质量为:8g+50g-55.36g=2.64g;
(3)解:设石灰石样品中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 2.64g

x=6g
石灰石样品中碳酸钙的质量分数为: ×100%=75%
×100%=75%
故答案为:(1)SiO2、CaCl2、HCl、H2O;(2)2.64g;(3)答:石灰石样品中碳酸钙的质量分数为75%;
分析:(1)根据反应进行后的生成物以及不反应的物质情况分析解答;
(2)根据质量守恒定律计算生成二氧化碳的质量即可;
(3)利用所得的二氧化碳质量利用方程式即可计算碳酸钙的质量,从而可得该石灰石样品中碳酸钙的质量分数;
点评:利用质量守恒定律求出反应放出二氧化碳的质量,是进行后面计算的基础,体现出运用知识分析问题的能力.
(2)由质量守恒定律可知该反应生成的二氧化碳质量为:8g+50g-55.36g=2.64g;
(3)解:设石灰石样品中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 2.64g

x=6g
石灰石样品中碳酸钙的质量分数为:
 ×100%=75%
×100%=75%故答案为:(1)SiO2、CaCl2、HCl、H2O;(2)2.64g;(3)答:石灰石样品中碳酸钙的质量分数为75%;
分析:(1)根据反应进行后的生成物以及不反应的物质情况分析解答;
(2)根据质量守恒定律计算生成二氧化碳的质量即可;
(3)利用所得的二氧化碳质量利用方程式即可计算碳酸钙的质量,从而可得该石灰石样品中碳酸钙的质量分数;
点评:利用质量守恒定律求出反应放出二氧化碳的质量,是进行后面计算的基础,体现出运用知识分析问题的能力.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
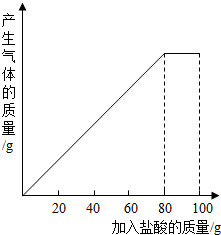 有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:
有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(2)石灰石样品中CaCO3质量分数为多少?(结果精确到0.1%)
(3)10%的CaCl2溶液可作为路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰右粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
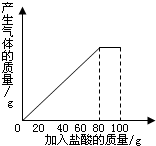 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(1)第2次加入盐酸后,a为
(2)石灰石样品中钙元素、碳元素和氧元素的质量比为多少?(结果用最简整数比表示)
(3)10%的CaCl2溶液可作路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据;
欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,请计算:这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | 25 | 20 | 15 | 15 |
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不溶于水也不与盐酸反应),得到如下表部分数据.
请计算:
(1)第2次加入盐酸后,a为 g.
(2)石灰石样品中碳酸钙的质量分数为多少?
(3)10%的CaCl2溶液可作路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
(4)画出35g石灰石样品中加入盐酸的质量与剩余固体的质量变化关系的示意图(在“答题卡”框图中作图)
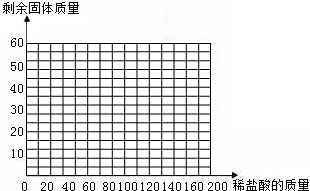
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 | 15 | 15 |
(1)第2次加入盐酸后,a为
(2)石灰石样品中碳酸钙的质量分数为多少?
(3)10%的CaCl2溶液可作路面保湿剂.欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)
(4)画出35g石灰石样品中加入盐酸的质量与剩余固体的质量变化关系的示意图(在“答题卡”框图中作图)
