题目内容
运载火箭的动力可由高氯酸铵(NH4ClO4)分解提供.化学方程式为2NH4Cl04
N2↑+Cl2↑+4X↑+202↑,下列有关说法不正确的是( )
| ||
| A、反应前后氧元素的化合价发生了改变 |
| B、生成的氮气和氧气的质量比为1:2 |
| C、X的化学式为H2O |
| D、D该反应属于分解反应 |
考点:质量守恒定律及其应用,有关元素化合价的计算,反应类型的判定
专题:化学用语和质量守恒定律
分析:A.反应前NH4Cl04中氧元素的化合价为-2价,反应后02中氧元素的化合价为0,发生了改变;
B.根据生成的氮气和氧气的质量比来分析解答;
C.根据化学变化前后原子的种类、数目不变,由反应的化学方程式2NH4ClO4
N2↑+Cl2↑+4X↑+2O2↑,推断反应中生成物X的分子构成,然后确定X物质的化学式.
D.根据分解反应的定义分析解答;
B.根据生成的氮气和氧气的质量比来分析解答;
C.根据化学变化前后原子的种类、数目不变,由反应的化学方程式2NH4ClO4
| ||
D.根据分解反应的定义分析解答;
解答:解:A.反应前NH4Cl04中氧元素的化合价为-2价,反应后02中氧元素的化合价为0,发生了改变;正确;
B.生成的氮气和氧气的质量比为:14×2:16×2×2=7:16;错误;
C.由反应的化学方程式2NH4ClO4
N2↑+Cl2↑+4X↑+2O2↑,可知:
反应前 反应后
N原子 2 2
H原子 8 0
Cl原子 2 2
O原子 8 4
根据化学变化前后原子的种类、数目不变,可判断生成物X的4个分子中含有8个H原子和4个O原子,则每个X的分子由2个H原子和1个O原子构成,物质X的化学式为H2O;
D.根据化学反应化学方程式为2NH4Cl04
N2↑+Cl2↑+4X↑+202↑,可知该反应为“一分多”是分解反应;
答案:B
B.生成的氮气和氧气的质量比为:14×2:16×2×2=7:16;错误;
C.由反应的化学方程式2NH4ClO4
| ||
反应前 反应后
N原子 2 2
H原子 8 0
Cl原子 2 2
O原子 8 4
根据化学变化前后原子的种类、数目不变,可判断生成物X的4个分子中含有8个H原子和4个O原子,则每个X的分子由2个H原子和1个O原子构成,物质X的化学式为H2O;
D.根据化学反应化学方程式为2NH4Cl04
| ||
答案:B
点评:根据化学变化前后原子的种类、数目不变,由反应的化学方程式,可以推断反应中某物质的分子构成及物质化学式的确定.

练习册系列答案
相关题目
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )


| A、此反应有单质 |
| B、化学变化的实质是原子进行重新组合 |
| C、该反应既不是化合反应,也不是分解反应 |
| D、参加反应的两种分子的个数比为2:3 |
 如图是实验室制取气体的部分装置.
如图是实验室制取气体的部分装置.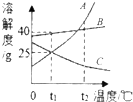 A、B、C三种固体物质的溶解度曲线如图所示.
A、B、C三种固体物质的溶解度曲线如图所示.