题目内容
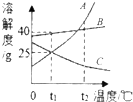 A、B、C三种固体物质的溶解度曲线如图所示.
A、B、C三种固体物质的溶解度曲线如图所示.①t1℃时,A、B、C的溶解度大小关系是
②t2℃时,将A、B、C各25g分别放入100g水中,能形成饱和溶液的物质是
③t2℃时,分别将A、C两种物质的饱和溶液各100g降温至t1℃后,所得溶液的溶质质量分数的大小关系是
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:①据溶解度曲线可比较同一温度下物质的溶解度大小;
②据t2℃时三种物质的溶解度分析解答,并结合饱和溶液、不饱和溶液的转化措施分析解答;
③据物质的溶解度随温度的变化及饱和溶液中溶质的质量分数分析判断.
②据t2℃时三种物质的溶解度分析解答,并结合饱和溶液、不饱和溶液的转化措施分析解答;
③据物质的溶解度随温度的变化及饱和溶液中溶质的质量分数分析判断.
解答:解:①由A、B、C三种固体物质的溶解度曲线可知,在t1℃时,A、B、C的溶解度大小关系是:B>A=C;
②观察溶解度曲线可知:t2℃时,AB的溶解度大于25g,C的溶解度小于25g,所以将A、B、C三种物质各25g分别放入100g水中,充分溶解后,能形成饱和溶液的是C;C的溶解度随温度的升高而降低,所以将其转化为不饱和溶液可采用降温、加水的方法;
③由A、C的溶解度曲线可知,A的溶解度随温度的降低而减小,C的溶解度随温度的降低而增大.当t2℃时,分别将A、C两种物质的饱和溶液各100g降温至t1℃后,A有晶体析出变为t1℃的饱和溶液,C变为t1℃的不饱和溶液,溶质质量分数不变.由于t1℃时A的溶解度大于在t2℃时C的溶解度,所以由溶质质量分数大小根据饱和溶液中溶解度越大溶质的质量分数越大可知,所得溶液的溶质质量分数的大小关系是:A>C.
故答案为:①B>A=C;②C;降温;加水;③A>C.
②观察溶解度曲线可知:t2℃时,AB的溶解度大于25g,C的溶解度小于25g,所以将A、B、C三种物质各25g分别放入100g水中,充分溶解后,能形成饱和溶液的是C;C的溶解度随温度的升高而降低,所以将其转化为不饱和溶液可采用降温、加水的方法;
③由A、C的溶解度曲线可知,A的溶解度随温度的降低而减小,C的溶解度随温度的降低而增大.当t2℃时,分别将A、C两种物质的饱和溶液各100g降温至t1℃后,A有晶体析出变为t1℃的饱和溶液,C变为t1℃的不饱和溶液,溶质质量分数不变.由于t1℃时A的溶解度大于在t2℃时C的溶解度,所以由溶质质量分数大小根据饱和溶液中溶解度越大溶质的质量分数越大可知,所得溶液的溶质质量分数的大小关系是:A>C.
故答案为:①B>A=C;②C;降温;加水;③A>C.
点评:本题结合溶解度曲线考查了溶解度曲线的应用,解答时要在掌握溶解度的概念、饱和溶液中溶质质量分数的计算方法的基础上分析解答,能较好考查学生分析解决问题的能力,同时考查了溶液配制的相关知识.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
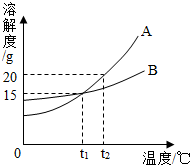 如图为A、B两种固体物质的溶解度曲线,下列说法中错误的是.( )
如图为A、B两种固体物质的溶解度曲线,下列说法中错误的是.( )| A、t1℃时,A、B的溶解度相等 |
| B、t1℃时,A的饱和溶液与B的饱和溶液的溶质的质量相等 |
| C、A的溶解度受温度的影响比B的溶解度受温度的影响大 |
| D、t2℃时,A、B的饱和溶液降温至t1℃时,它们的溶质的质量分数都变小 |
 分别表示A和B两种不同原子,下图能表示“2A2”的是( )
分别表示A和B两种不同原子,下图能表示“2A2”的是( )A、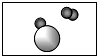 |
B、 |
C、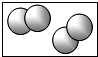 |
D、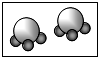 |
运载火箭的动力可由高氯酸铵(NH4ClO4)分解提供.化学方程式为2NH4Cl04
N2↑+Cl2↑+4X↑+202↑,下列有关说法不正确的是( )
| ||
| A、反应前后氧元素的化合价发生了改变 |
| B、生成的氮气和氧气的质量比为1:2 |
| C、X的化学式为H2O |
| D、D该反应属于分解反应 |
下列物质中氮元素的化合价最低的是( )
| A、N2 |
| B、NH3 |
| C、N2O5 |
| D、NO2 |