题目内容
2.根据图示回答问题.
(1)实验室可以用一种盐类物质制取氧气,选用的发生装置是A(填标号),反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(2)实验室用石灰石(杂质既不溶于水也不与稀盐酸反应)和稀盐酸反应制取二氧化碳.选用发生装置B中长颈漏斗末端要伸入液面下的理由是防止气体外逸.
(3)实验结束后,锥形瓶内已无气泡产生,但还有少量固体剩余.小文和小明对锥形瓶内溶液中溶质的成分展开辩论:
①小文说:因为瓶内有固体剩余,所以溶液中只有氯化钙而无盐酸.小明不完全同意小文说法,请你说出小明的理由剩余固体可能完全是杂质,而杂质不与盐酸反应,所以溶液中盐酸可能已过量.
②按小明的猜想,写出溶液中溶质成分的两种可能CaCl2、HCl;CaCl2.
分析 (1)实验室中常利用加热氯酸钾(盐类)来制取氧气,此装置是加热固体型,纯氧能使带火星的木条复燃,据此解答即可;
(2)实验室制取二氧化碳,需要利用大理石与稀盐酸反应,据此书写化学反应方程式;
依据杂质成分分析解答即可.
解答 解:
(1)选用加热氯酸钾制取氧气,此此装置是加热固体型,故选择A,化学反应方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)实验室中制取二氧化碳,利用的是大理石与稀盐酸,化学反应方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,选用发生装置B中长颈漏斗末端要伸入液面下的理由是防止气体外逸,故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑,防止气体外逸;
①若剩余固体中有不与盐酸反应的,那么盐酸加入过量,无现象,故答案为:剩余固体可能完全是杂质,而杂质不与盐酸反应,所以溶液中盐酸可能已过量;
②按照小明的猜想,溶液中可能含有CaCl2、HCl或者仅有:CaCl2,答案为:CaCl2、HCl;CaCl2.
答案:
(1)A,2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)防止气体外逸,
①剩余固体可能完全是杂质,而杂质不与盐酸反应,所以溶液中盐酸可能已过量
②CaCl2、HCl CaCl2
点评 本题主要考查的是实验室中氧气的制法与二氧化碳的实验室制法,综合性较强,难度不大.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
13.下列物质分别放入水里,滴加无色酚酞试液能变红的是( )
| A. | 生石灰 | B. | 食盐 | C. | 硫酸铜 | D. | 氢氧化铜 |
10.小明在家中探究食用白醋的性质,选用了家庭生活中的下列常见物品:200ml的软透明塑料瓶、食品干燥剂、白醋、鸡蛋壳、紫罗兰花、锈铁钉、蒸馏水、纯碱、玻璃小杯.
【问 题】
白醋是否具有酸类的性质?
【查阅资料】
(1)白醋为无色透明液体,其主要成分是醋酸,化学式可表示为HAc,Ac-代表醋酸根;
(2)食品干燥剂的主要成分是氧化钙;
(3)紫罗兰花遇酸变为红色;
(4)醋酸盐中除银盐和汞盐外都易溶解于水.
【探究与验证】(请你帮助填写表中空白)
【反思与评价】
(1)小明将干燥剂袋口打开一段时间后,袋中的白色颗粒粘在了一起,请写出变化的化学方程式CaO+H2O═Ca(OH)2.
(2)上面“实验结论”中,错误的是(填实验序号)四.
(3)上述实验三的现象还不足以得出表中所述的相应结论,为此还需要补充相应的实验,写出该实验发生反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
【问 题】
白醋是否具有酸类的性质?
【查阅资料】
(1)白醋为无色透明液体,其主要成分是醋酸,化学式可表示为HAc,Ac-代表醋酸根;
(2)食品干燥剂的主要成分是氧化钙;
(3)紫罗兰花遇酸变为红色;
(4)醋酸盐中除银盐和汞盐外都易溶解于水.
【探究与验证】(请你帮助填写表中空白)
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 一 | 将白醋滴在紫罗兰花上 | 紫罗兰花变红 | 白醋的pH<7 |
| 二 | 将锈铁钉放在小玻璃杯中,加入白醋 | 刚开始时铁锈溶解,溶液由无色变成黄色,一段时间后,有气泡冒出 | 1.白醋能与铁锈反应 2.白醋能与铁反应 |
| 三 | 向软塑料瓶中加入10ml白醋,将瓶捏扁,加入约5g鸡蛋壳,拧紧瓶盖 | 瓶中有气泡冒出,扁塑料瓶逐渐膨胀 | 白醋能与碳酸钙反应放出CO2 |
| 四 | 向白醋中加入纯碱 | 白醋中有气泡冒出 | 白醋能与碱反应 |
(1)小明将干燥剂袋口打开一段时间后,袋中的白色颗粒粘在了一起,请写出变化的化学方程式CaO+H2O═Ca(OH)2.
(2)上面“实验结论”中,错误的是(填实验序号)四.
(3)上述实验三的现象还不足以得出表中所述的相应结论,为此还需要补充相应的实验,写出该实验发生反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
7.葡萄糖是重要的搪类物质,其化学式为C6H12O6,下列有关叙述错误的是( )
| A. | 葡萄糖由三种原子构成 | |
| B. | 它属于有机物 | |
| C. | 葡萄糖中碳氢氧三种元素的质量比6:1:8 | |
| D. | 在人体组织里,葡萄糖在酶的作用下经缓慢氧化转变成二氧化碳和水 |
12.燃烧是生活中常见的一种现象,下列说法正确的是( )
| A. | 氢气燃烧时将化学能转化为热能 | |
| B. | 烧火时把木柴架空的目的是降低着火点 | |
| C. | 可燃物只要达到着火点就能燃烧 | |
| D. | 煤燃烧产生CO2是形成酸雨的主要原因 |

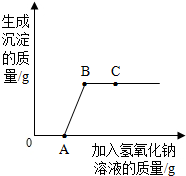 将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题:
将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题: