题目内容
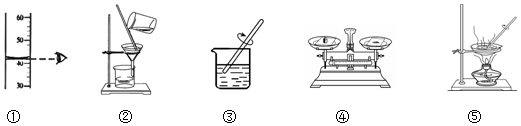
4.下列装置常用于实验室制取气体,根据给出的装置回答下列问题:
(1)指出编号仪器名称:②长颈漏斗.
(2)实验室利用A装置制取氧气,反应原理用化学方程式表示为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.利用C装置收集氧气的最佳时刻是气泡连续均匀冒出时收集.用收集到的氧气完成硫粉燃烧实验后,还需向集气瓶内加入适量氢氧化钠溶液,目的是SO2+2NaOH=Na2SO3+H2O(用化学方程式表示).
(3)制取并收集二氧化碳应选择的装置是BE,使用该套发生装置制取气体的突出优点是可以控制反应的发生和停止.若改用F装置收集二氧化碳,则气体应从b端进入.制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲用G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→e→f→c→d(用端口字母表示).
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,用排水法收集氧气的最佳时刻是气泡连续均匀冒出时收集,二氧化硫和氢氧化钠反应生成亚硫酸钠和水进行分析;
(3)根据实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳的密度比空气大,溶于水,通过装置内压强的改变可以实现固体和液体的分离,二氧化碳密度比空气大,饱和碳酸氢钠可以吸收氯化氢,浓硫酸有吸水性,洗气时应该是长进短出进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,②是长颈漏斗;
(2)氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,用排水法收集氧气的最佳时刻是气泡连续均匀冒出时收集,二氧化硫和氢氧化钠反应生成亚硫酸钠和水,化学方程式为:SO2+2NaOH=Na2SO3+H2O;
(3)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳的密度比空气大,溶于水,所以制取并收集二氧化碳应选择的装置是BE,通过装置内压强的改变可以实现固体和液体的分离,所以使用该套发生装置制取气体的突出优点是:可以控制反应的发生和停止,二氧化碳密度比空气大,所以改用F装置收集二氧化碳,则气体应从b端进入,饱和碳酸氢钠可以吸收氯化氢,浓硫酸有吸水性,洗气时应该是长进短出,所以装置正确的连接顺序是:混合气体→e→f→c→d.
故答案为:(1)长颈漏斗;
(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,气泡连续均匀冒出时收集,SO2+2NaOH=Na2SO3+H2O;
(3)BE,可以控制反应的发生和停止,b,e→f→c→d.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

(1)设计实验证明空气中含有水取一些冰块放入一只干燥的烧杯中,一会儿发现烧杯外壁有水滴出现.
(2)设计实验证明空气中含有二氧化碳将盛有半杯澄清石灰水的烧杯敞口放置,一段时间后澄清石灰水水面出现一薄层白色固体.
(3)为了比较人呼出的气体和吸入的空气中二氧化碳含量的高低,向盛满呼出气体的集气瓶内滴入数滴澄清石灰水,盖上玻璃片振荡,他接下来应选择的对比实验是B.
A.在盛满空气的集气瓶内滴入相同滴数的石灰水,敞口放置;
B.在盛满空气的集气瓶内滴入相同滴数的石灰水,盖上玻璃片振荡.
(4)请帮助小明填写关于酒精燃烧探究的实验报告:
| 实验现象 | 实验结论 |
| 把一只干燥的冷烧杯罩在酒精灯上,观察到烧林内壁 出现水雾 | 说明酒精燃烧时生成了水 |
| 用手触摸上一步骤中的烧杯底部,感觉发热(或发烫) | 说明酒精燃烧时有热量放出 |
| 用内壁涂有澄清石灰水的烧杯罩在火焰上,发现烧杯 内壁澄清的石灰水变浑浊 | 说明呼出的气体中含有二氧化碳 |
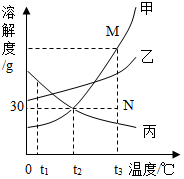 如图是甲、乙、丙三种物质的溶解度曲线,回答问题:
如图是甲、乙、丙三种物质的溶解度曲线,回答问题: