题目内容
11.下列五组物质,每组中有一种物质从某种角度分析与其它四种不同,请找出该物质,并说明理由.(1)Fe、S、C、PFe,
(2)H2、O2、N2、SS,
(3)Fe2O3、NaCl、CuO、H2ONaCl,
(4)AgCl、BaSO4、KNO3、CaCO3KNO3,
(5)CuSO4、FeCl3、KMnO4、K2CO3K2CO3.
分析 (1)依据元素类别分析;
(2)依据单质构成分析;
(3)依据化合物组成元素分析判断;
(4)根据盐的溶解性分析;
(5)根据盐的颜色分析.
解答 解:(1)Fe属于金属元素形成的单质,S、C、P属于非金属元素形成的单质;
故答案为:Fe;
(2)H2、O2、N2都是双原子分子,S不是双原子分子;
故答案为:S;
(3)Fe2O3、H2O、CuO都是由两种元素组成且其中一种是氧元素的化合物,属于氧化物,NaCl不是氧化物;
故答案为:NaCl;
(4)AgCl、BaSO4、CaCO3,属于难溶的盐,KNO3是易溶于水的盐;
故答案为:KNO3;
(5)CuSO4、FeCl3、KMnO4都是有颜色的盐,K2CO3 属于无色晶体;
故答案为:K2CO3.
点评 本题考查物质的分类,题目难度不大,注意酸、碱、盐以及氧化物,的概念的区别和联纯净物和混合物、单质和化合物的区别联系.

练习册系列答案
相关题目
1.除去下列物质中混有的少量杂质,所选用的试剂及操作方法错误的是( )
| 序号 | 物质 | 杂质(少量) | 除去杂质的方法 |
| A | O2 | 水蒸气 | 通过生石灰 |
| B | C粉 | 氧化铜 | 加入过量稀盐酸,过滤 |
| C | 氯化钙溶液 | 稀盐酸 | 加入过量氢氧化钙溶液,过滤 |
| D | NaCl溶液 | Na2CO3 | 加入稀硫酸至不再产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
2.在H2O、H2O2、H2SO4三种分子中都含有( )
| A. | 氢气 | B. | 氢原子 | C. | 氢分子 | D. | 氢元素 |
6.下列数据是相应物质的近似pH,其中一定呈碱性的是( )
| A. |  (9.5~10.5)液体肥皂 | B. |  (3.3~5.2 )菠萝汁 | ||
| C. |  (2.0~3.0)柠檬汁 | D. |  (6.5~7.5)饮用水 |
16.如图所示4个坐标图分别表示4个实验过程中某些量的变化,其中正确的是.
| A. |  向盐酸中加入水 | B. |  10 mL 5%的H2O2溶液分解 | ||
| C. |  将饱和石灰水升温 | D. | 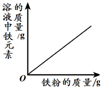 向一定量的稀盐酸中加入铁粉 |
3.二氧化氯是一种高效消毒剂在2003年防止“非典”工作中起到了重要作用.KClO3和浓盐酸在一定温度下会生成二氧化氯2KClO3+4HCl(浓)═2KCl+2ClO2↑+Cl2↑+2H2O浓盐酸在反应中显示出来的性质是 ( )
| A. | 只有还原性 | B. | 还原性和酸性 | C. | 只有氧化性 | D. | 氧化性和酸性 |
20.物质都是由微观粒子构成的,下列物质由原子构成的是( )
| A. | 金刚石 | B. | 氯化钠 | C. | 水 | D. | 氢气 |

