题目内容
已知一种固体化合物由C、H、O、Cu四种元素组成.向盛有该化合物的试管中加入稀盐酸,产生大量气泡,固体逐渐溶解,得到蓝绿色溶液.己知这种蓝绿色是氯化铜溶液.
(1)探究产生的气体是什么.
[猜想]①可能是氢气;②________③________……
[实验]请针对你②和③猜想中的一种,设计实验,验证你的猜想.________.
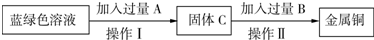
(2)从蓝绿色溶液中提取金属铜.现利用该溶液制取金属铜,过程如下:
操作1的名称为________,完成该实验需要的主要仪器有________,加入过量的A的目的是________,反应化学方程式为________.
②加入足量B的目的是________,如何确定此目的已经达到?________.
答案:
解析:
解析:
|
(1)可能是氧气;可能是二氧化碳(或答可能是一氧化碳、甲烷等也正确).用带火星的木条试验,木条复燃,证明是氧气;(或将气体通入澄清的石灰水,石灰水变浑浊,证明是二氧化碳;或将气体点火,气体能燃烧,用干而冷的烧杯罩在火焰上,烧杯内壁出现水珠,迅速将烧杯倒过来,注入少量澄清石灰水,石灰水变浑浊,证明是甲烷). (2)①过滤带铁圈的铁架台、漏斗、玻璃棒、烧杯 使溶液中的氯化铜完全反应 Fe+CuCl2=FeCl2+Cu(或Zn+CuCl2=ZnCl2+Cu等,答案合理即可) ②完全除去过量的A 溶液中不再有气泡产生,则说明目的已经达到. |

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目