题目内容
19.葡萄糖酸锌(C12H22O14Zn)中共含有四种元素,其中所含人体必需的微量元素是Zn,碳、氢元素的质量比是72:11;2015年诺贝尔奖获得者屠呦呦发现的青蒿素是一种抗疟疾药,若14.1g青蒿素完全燃烧生成33.0gCO2和9.9gH2O,则青蒿素中氧的质量与其完全燃烧消耗氧气的质量之比为5:36(以上结果均取最简整数比).分析 根据物质的组成、微量元素的种类以及化合物中元素质量比的计算方法分析;根据质量守恒定律进行分析解答.
解答 解:葡萄糖酸锌(C12H22O14Zn)是由碳、氢、氧、锌四种元素组成的;其中含有人体必需的微量元素是Zn;碳、氢、氧属于常量元素;葡萄酸锌中碳、氢元素的质量比为(12×12):(1×22)=72:11.
由质量守恒定律可知,青蒿素中含碳元素的质量与33.0g二氧化碳中碳元素的质量相等,为:33.0g×$\frac{12}{44}$×100%=9.0g;
青蒿素中氢元素的质量与9.9g水中氢元素的质量相等,为:9.9g×$\frac{1×2}{18}×100%$=1.1g;
则青蒿素中含氧元素的质量为:14.1g-9.0g-1.1g=4g
参加反应的氧气的质量为:33.0g+9.9g-14.1g=28.8g
青蒿素中氧的质量与其燃烧消耗氧气的质量之比为:4g:28.8g=5:36.
故答案为:四;Zn;72:11;5:36.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
10.下列物质属于纯净物的是( )
| A. | 雪碧饮料 | B. | 食醋 | ||
| C. | 加碘食盐 | D. | 含铁70%的氧化铁样品 |
7.由软锰矿(主要成分为MnO2)制备KMnO4反应流程可表示如下,下列说法正确的是( )
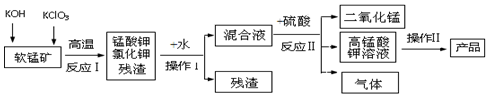

| A. | MnO2可循环利用 | |
| B. | 反应 I中无元素化合价变化 | |
| C. | 操作Ⅰ和操作Ⅱ是相同的操作 | |
| D. | 反应Ⅱ是3K2MnO4+2H2SO4=MnO2↓+2KMnO4+2H2O+2X,则X是K2SO4 |
8. 分别点燃两根火柴,其中一根火柴头竖直向上,另一根火柴头向下倾斜,小明发现火柴头向下倾斜的容易持续燃烧,另一根则不能.该现象说明燃烧的条件是( )
分别点燃两根火柴,其中一根火柴头竖直向上,另一根火柴头向下倾斜,小明发现火柴头向下倾斜的容易持续燃烧,另一根则不能.该现象说明燃烧的条件是( )
 分别点燃两根火柴,其中一根火柴头竖直向上,另一根火柴头向下倾斜,小明发现火柴头向下倾斜的容易持续燃烧,另一根则不能.该现象说明燃烧的条件是( )
分别点燃两根火柴,其中一根火柴头竖直向上,另一根火柴头向下倾斜,小明发现火柴头向下倾斜的容易持续燃烧,另一根则不能.该现象说明燃烧的条件是( )| A. | 物质具有可燃性 | B. | 可燃物与充足氧气接触 | ||
| C. | 可燃物温度达到着火点 | D. | 可燃物硬度小 |
5.小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质的质量分数为10%,具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙、氯化钠、氢氧化钙或是碳酸钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是常温下不可能得到质量分数为10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞溶液(填“紫色石蕊溶液”或“无色酚酞溶液”),试液边红色,该溶液不可能是氯化钠.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择BaCl2溶液来确定该溶液的成份;
方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】小亮选择了方案甲进行实验:
(4)【实验反思】①有同学认为还可以用一种常见的碱溶液来确定,那么它可能是Ca(OH)2溶液;
②小亮经过反思,向同学们提出如下建议,你认为合理的是A
A.倾倒液体时,应注意保护标签不被腐蚀 B.无法辨认的药品,直接倒掉,无需保留.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是常温下不可能得到质量分数为10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞溶液(填“紫色石蕊溶液”或“无色酚酞溶液”),试液边红色,该溶液不可能是氯化钠.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择BaCl2溶液来确定该溶液的成份;
方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】小亮选择了方案甲进行实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加BaCl2溶液. | 该溶液是碳酸钠溶液. 有关反应方程式为:BaCl2+Na2CO3═BaCO3↓+2NaCl |
②小亮经过反思,向同学们提出如下建议,你认为合理的是A
A.倾倒液体时,应注意保护标签不被腐蚀 B.无法辨认的药品,直接倒掉,无需保留.
 江西即将迎来高铁时代,赣州到南昌的高铁将于2019年建成,届时赣州到南昌只需2小时.
江西即将迎来高铁时代,赣州到南昌的高铁将于2019年建成,届时赣州到南昌只需2小时. 生活中科学之美、科学之趣随处可见.如图是某厂商设计的T恤,T恤上有趣的图案是邻二溴苯(C6H4Br2)分子的结构简式.
生活中科学之美、科学之趣随处可见.如图是某厂商设计的T恤,T恤上有趣的图案是邻二溴苯(C6H4Br2)分子的结构简式.