题目内容
某温度下,有两杯浓度完全相同的NaCl溶液,第一杯蒸发a g水,析出m g晶体;第二杯蒸发b g水,析出n g晶体,求NaCl在该温度下的溶解度.(假设a<b)
考点:固体溶解度的概念
专题:溶液、浊液与溶解度
分析:氯化钠的溶解度计算时要看溶液是饱和溶液才能计算,一开始溶液不一定饱和,根据两次蒸发的差值考虑.
解答:解:恒温蒸发bg水,析出ng晶体.是在恒温蒸发ag水,得到mg晶体后又蒸发(b-a)g,析出(n-m)g晶体,所以蒸发(b-a)g,析出(n-m)g晶体是饱和溶液的蒸发,即(b-a)g水中只能溶解(n-m)g.
设某温度下NaCl在该温度下的溶解度为sg.
则:sg:100g=(n-m)g:(b-a)g
s=
g
答:某温度下NaCl在该温度下的溶解度为
g.
设某温度下NaCl在该温度下的溶解度为sg.
则:sg:100g=(n-m)g:(b-a)g
s=
| 100(n-m) |
| b-a |
答:某温度下NaCl在该温度下的溶解度为
| 100(n-m) |
| b-a |
点评:解答本题的关键是知道溶解度是在该温度下100g水中最多溶解的溶质质量.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
夏飞同学在化学课上提出,可用澄清石灰水来检验人呼出的气体中是否含有二氧化碳,就这一过程而言,属于科学探究环节中的( )
| A、提出假设 | B、收集证据 |
| C、设计实验 | D、做出结论 |
下列叙述正确的是( )
| A、1 mol H2SO4 的物质的量是98g/mol |
| B、H2SO4 的摩尔质量为98 |
| C、0.5mol的氧 |
| D、6.02×1022个 H2SO4 分子的质量为9.8g |
生活中可能遇到下列混合物,能按“溶解-过滤-蒸发”的步骤加以分离的是( )
| A、食盐和细砂 |
| B、纯碱和烧碱 |
| C、水和酒精 |
| D、CaCO3和Mg(OH)2 |
下列叙述正确的是( )
| A、1 mol CO2 的质量为44g/mol |
| B、CO2的摩尔质量为44g |
| C、CO2的摩尔质量等于CO2的相对分子质量 |
| D、NA个CO2的质量与CO2的相对分子质量在数值上相同 |
 ,它的核内有
,它的核内有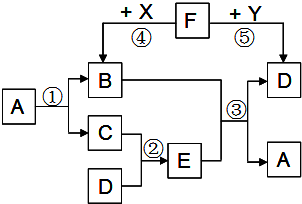
 构建知识网络是一种重要的学习方法.如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题:
构建知识网络是一种重要的学习方法.如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题: