题目内容
17.在游览中她看到了一座铁索桥.(1)联系所学金属冶炼的知识,提出了下列问题.
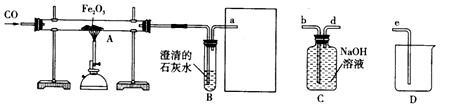
①工业上用一氧化碳和赤铁矿炼铁的原理是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(写化学方程式).
②建造这座桥大约用了112吨铁,理论需要氧化铁160吨.
(2)走过铁索桥后她发现有位游客不小心擦伤了手,她赶快拿出自带的碘酒帮其消毒.碘酒是将碘溶解在酒精中制得碘的酒精溶液,碘酒中的溶剂是酒精.
分析 (1)①工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,写出反应的化学方程式即可.
②根据质量守恒定律,反应前后铁元素质量不变,进行分析解答.
(2)根据碘酒是将碘溶解在酒精中制得碘的酒精溶液,进行分析解答.
解答 解:(1)①工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②由质量守恒定律,反应前后铁元素质量不变,建造这座桥大约用了112吨铁,理论需要氧化铁的质量为112t÷($\frac{56×2}{56×2+16×3}$×100%)=160t.
(2)碘酒是将碘溶解在酒精中制得碘的酒精溶液,碘是溶质,酒精是溶剂.
故答案为:(1)①Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;②160;(2)酒精.
点评 本题难度不大,掌握工业上炼铁的反应原理、溶质和溶剂的判别方法等是正确解答本题的关键.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
5.以下家庭制作中,发生了化学变化的是( )
| A. | 凉水冻冰 | B. | 葡萄酿酒 | C. | 萝卜风干 | D. | 辣椒剁碎 |
12.根据如图放入溶解度曲线,下列说法不正确的是( )


| A. | a点表示,t2℃时100g水中最多溶解甲物质25g | |
| B. | 甲物质的溶解度随温度的升高而增大 | |
| C. | t1℃时,甲、乙两物质的饱和溶液中含溶质的质量肯定相等 | |
| D. | t1℃时,甲、乙两物质的溶解度相等 |
2.下列物质的分类正确的是( )
| A. | 不锈钢和生理盐水属于纯净物 | B. | 液态氧属于氧化物 | ||
| C. | 乙醇属于有机物 | D. | 鸡蛋、水果属于蛋白质 |
9.下列校园运动设施和器材中,没有用到有机合成材料的是( )
| A. | 塑料跑道 | B. | 钢质单杠 | C. | 尼龙跳绳 | D. | 橡胶球 |
7.家庭用煤经过从“煤球”到“蜂窝煤”的变化,其目的是( )
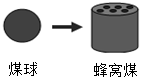

| A. | 增大可燃物的热值 | B. | 降低可燃物的着火点 | ||
| C. | 提高空气中氧气的含量 | D. | 增大可燃物与空气的接触面积 |