题目内容
20.竹炭包是一种集观赏与空气净化为一体的产品.这种产品可对车内及室内空气中的一氧化碳、甲醛等有害气体进行吸附.某课外小组对竹炭进行初步探究.【提出问题】竹炭中是否含有碳元素.
【猜想与假设】竹炭中含有碳元素
【查阅资料】①新鲜的血液,遇一氧化碳由鲜红变为暗红.
②氢氧化钠能与二氧化碳发生化学反应.
【设计实验】通过检验竹炭燃烧产物,证明竹炭中含有碳元素.所用装置如图1所示.
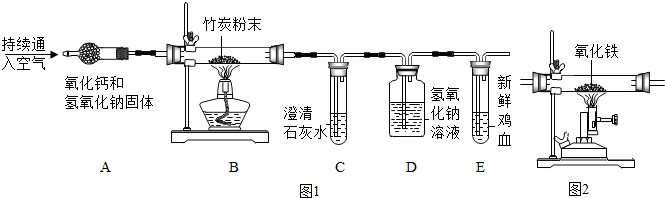
(1)A装置的作用为除去了空气中的水蒸汽和二氧化碳.
(2)实验开始后,C装置中产生白色沉淀,在白色沉淀中不断连续通入二氧化碳气体,结果白色沉淀消失,生成可溶性的碳酸氢钙{Ca(HCO3)2反应化学方程式为CO2+H2O+CaCO3=Ca(HCO3)2.
D装置的作用是:吸收生成的CO2,反应化学方程式为CO2+2NaOH=Na2CO3+H2O,
E装置中新鲜的鸡血变为暗红色,证明竹炭燃烧产物中有一氧化碳产生.
(3)小红认为应在A、B装置间,增加澄清石灰水,目的是检验二氧化碳是否除尽.
(4)小明认为可以用图2所示的装置,替换原装置中的E装置,你认为可以吗?主要原因是什么?不可以,因在E装置中通入的为一氧化碳和氧气混合气体,高温可能会爆炸.
【初步结论】竹炭中含有碳元素.
【拓展应用】竹炭细密多孔,牙膏中含有竹炭等成分具有消炎
止痛、化淤、去污等功效,下列有关竹炭牙膏的用途描述正确的B、C、D.
A.可防癌抗衰老 B.虫咬、灼伤可消炎止痛
C.可除去口中异味 D.可除衣领袖口等处的汗渍.
分析 【设计实验】A装置除去了空气中的水蒸汽和二氧化碳,B装置氧气与竹炭粉末在加热条件下发生反应,C装置检验反应的生成物中是否有二氧化碳,D装置除去反应生成的二氧化碳,E装置检验反应的生成物中是否有一氧化碳.
【拓展应用】根据“竹炭细密多孔”、“竹炭等成分具有消炎、止痛、化瘀、去污等功效”,推测选项.
解答 解:【设计实验】(1)由于空气中含有二氧化碳和水蒸气,A装置的作用为除去了空气中的水蒸汽和二氧化碳;
(2)实验开始后,C装置中产生白色沉淀,在白色沉淀中不断连续通入二氧化碳气体,结果白色沉淀消失,生成可溶性的碳酸氢钙Ca(HCO3)2,根据反应物:二氧化碳、水、碳酸钙,生成物为碳酸氢钙Ca(HCO3)2,则反应化学方程式为:CO2+H2O+CaCO3=Ca(HCO3)2.D装置的作用是:吸收生成的CO2,二者反应的化学方程式为 CO2+2NaOH=Na2CO3+H2O.因为新鲜的人或动物血液,遇一氧化碳由鲜红变为暗红,而本题中的实验现象是新鲜的鸡血变为暗红色,说明了竹炭燃烧产物中有一氧化碳产生.
(3)A、B装置间,增加澄清石灰水,若澄清的石灰水不变浑浊,可以确定空气中的二氧化碳已经除尽,不会对后面的实验造成干扰.
(4)通入E装置中的气体除了有一氧化碳外还有氧气,加热有可能会发生爆炸.所以不可以替换原装置中的E装置,因在E装置中通入的为一氧化碳和氧气混合气体,高温可能会爆炸.
【拓展应用】由牙膏中含有竹炭等成分具有消炎、止痛、化淤、去污等功效,可知竹炭牙膏的用途虫咬、灼伤可消炎止痛、可除去口中异味、可除衣领袖口等处的汗渍,而不具有防癌抗衰老的用途.
故选:B、C、D
故答案为:(1)除去空气中的CO2,防止干扰;
(2)CO2+H2O+CaCO3=Ca(HCO3)2;吸收生成的CO2;CO2+2NaOH=Na2CO3+H2O;反应生成CO
(3)证明空气中的二氧化碳气体已经除尽;
(4)不可以,因为CO气体中混有O2,会爆炸;B、C、D.
点评 检验一氧化碳最安全的方法是通入新鲜血液,若加热或点燃,都有可能发生爆炸的危险.

| A. | 用食盐水浸泡鸡蛋做无壳蛋 | B. | 用自制简易净水器除去水中异味 | ||
| C. | 用淬火后的缝衣针做钓鱼钩 | D. | 用铜导线和食醋制氢气 |
| A. | 鸡蛋放入醋中变成“软壳蛋” | B. | 用肥皂水区别硬水和软水 | ||
| C. | 用回火后的钢针作鱼钩 | D. | 用自来水清除盛石灰水瓶壁的白膜 |
| A. |  水的电解 | |
| B. |  红磷在密闭的容器内燃烧 | |
| C. |  一定量的过氧化氢和二氧化锰混合制氧气 | |
| D. |  等质量的锌、铁与足量的稀硫酸反应 |
| A. | CO2 | B. | Al2O3 | C. | Fe2O3 | D. | SiO2 |
| A. | C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO | B. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | ||
| C. | 2HClO$\frac{\underline{\;光\;}}{\;}$2HCl+O2↑ | D. | 2NaOH+H2SO4═Na2SO4+2H2O |
| A. | 组成CO、CO2的元素种类相同,所以它们的化学性质相同 | |
| B. | 成语“火上浇油”是指“油”可以使可燃物与氧气隔绝,达到灭火的目的 | |
| C. | “春色满园,花香四溢”说明分子在不停地运动 | |
| D. | 气体受热膨胀是因为温度升高气体分子变大 |
| 温度(℃) | 0 | 10 | 20 | 30 | 50 | 60 | 80 | 90 | 100 | |
| 溶解度 (g) | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 85.5 | 130 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 39.8 | |
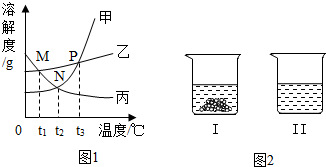
(2)现有60℃的硝酸钾饱和溶液230g,若要使其析出晶体84.2g,温度应降至30℃.
(3)硝酸钾和氯化钠在t℃时的溶解度均为S,根据上表中的数据分析可推知,S的数值所在的最小范围是36.0g<S<36.3g.
(4)20℃时,将等质量的KNO3和NaCl固体分别加入100g的水中,充分溶解,温度恢复到20℃,其结果如图2所示,有关说法中正确的是AC.
A.烧杯Ⅰ中溶解的是KNO3,烧杯Ⅱ中溶解的是NaCl
B.烧杯Ⅱ中的溶液是不饱和溶液
C.升高温度或加入溶剂都可使烧杯Ⅰ中的固体全部溶解
D.若将烧杯Ⅰ中溶液变成不饱和,其溶质的质量分数一定减小.