题目内容
10.现有KNO3和NaCl不同温度时的溶解度数据和溶解度曲线图.| 温度(℃) | 0 | 10 | 20 | 30 | 50 | 60 | 80 | 90 | 100 | |
| 溶解度 (g) | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 85.5 | 130 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 39.8 | |
(2)现有60℃的硝酸钾饱和溶液230g,若要使其析出晶体84.2g,温度应降至30℃.
(3)硝酸钾和氯化钠在t℃时的溶解度均为S,根据上表中的数据分析可推知,S的数值所在的最小范围是36.0g<S<36.3g.
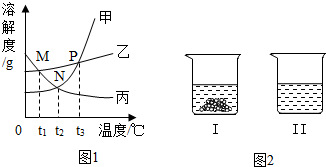
(4)20℃时,将等质量的KNO3和NaCl固体分别加入100g的水中,充分溶解,温度恢复到20℃,其结果如图2所示,有关说法中正确的是AC.
A.烧杯Ⅰ中溶解的是KNO3,烧杯Ⅱ中溶解的是NaCl
B.烧杯Ⅱ中的溶液是不饱和溶液
C.升高温度或加入溶剂都可使烧杯Ⅰ中的固体全部溶解
D.若将烧杯Ⅰ中溶液变成不饱和,其溶质的质量分数一定减小.
分析 根据物质的溶解度表和溶解度曲线可以判断某种物质的溶解度曲线;
根据析出晶体的质量可以判断温度的降低范围;
根据溶解度表可以判断相关方面的问题;
20℃时氯化钠的溶解度大于硝酸钾的溶解度.
解答 解:(1)硝酸钾和氯化钠的溶解度都是随着温度的升高而增大,硝酸钾的溶解度受温度变化影响大,因此图1中表示KNO3的溶解度曲线图是甲.
故填:甲.
(2)60℃时硝酸钾的溶解度是130g,硝酸钾饱和溶液230g中含有130g硝酸钾和100g水,若要使其析出晶体84.2g,温度应降至30℃.
故填:30℃.
(3)硝酸钾和氯化钠在t℃时的溶解度均为S,根据上表中的数据分析可推知,S的数值所在的最小范围是36.0g<S<36.3g.
故填:36.0g<S<36.3g.
(4)A.因为20℃时氯化钠的溶解度大于硝酸钾的溶解度,因此烧杯Ⅰ中溶解的是KNO3,烧杯Ⅱ中溶解的是NaCl,该选项说法正确;
B.烧杯Ⅱ中的溶液可能是不饱和溶液,也可能是饱和溶液,该选项说法不正确;
C.因为硝酸钾的溶解度随着温度的升高而增大,所以升高温度或加入溶剂都可使烧杯Ⅰ中的固体全部溶解,该选项说法正确;
D.若将烧杯Ⅰ中溶液变成不饱和,其溶质的质量分数可能减小,也可能增大,该选项说法不正确.
故填:AC.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
1.物质的溶液,根据它们自身的性质和相互间的反应现象,不用其它试剂就可以加以鉴别的是( )
| A. | FeCl3 NaCl Ba(OH)2 | B. | KCl HCl NaNO3 | ||
| C. | Na2SO4 HCl H2SO4 | D. | CuCl2 NaNO3 K2SO4 |
18.下列过程涉及到的变化主要是化学变化的是( )
| A. | 纸张燃烧 | B. | 雪化成水 | C. | 榨取果汁 | D. | 海水晒盐 |
5.下列说法中,错误的是( )
| A. | 燃烧煤容易造成空气污染,所以应禁止通过燃烧煤来提供能源 | |
| B. | 在煤、石油、天然气等三大化石燃料中,天然气是相对清洁的能源 | |
| C. | 垃圾分类回收既可以充分利用资源又可以减少环境污染 | |
| D. | 用肥皂水区分硬水和软水时,泡沫多的是软水,泡沫少的是硬水 |
15.如图所示的实验操作中,完全正确的是( )
| A. | 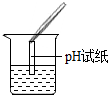 测定溶液pH | B. | 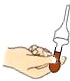 取用液体药品 | C. | 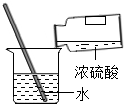 稀释浓硫酸 | D. |  加入大理石 |
2.图中参加反应的甲、乙分子和生成的丙分子的个数比为( )
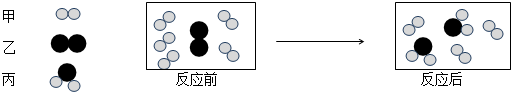

| A. | 5:1:2 | B. | 2:1:2 | C. | 3:1:2 | D. | 1:1:2 |
19.下列说法正确的是( )
| A. | 氢气在空气中燃烧,其变化的最小粒子是氢分子和氧分子 | |
| B. | 水是一种氧化物,含有氧元素,因此含有氧元素的化合物都是氧化物 | |
| C. | 空气的主要成分是氮气和氧气,因此组成空气的成分都属于单质 | |
| D. | 铁、水和氯化钠分别是由原子、分子和离子构成 |
2.下列变化属于物理变化的是( )
| A. |  工业炼铁 | B. |  榨鲜果汁 | C. |  煤炭燃烧 | D. |  炸药爆破 |