题目内容
14.请回忆你学习过程的“质量守恒定律”的实验探究,并按要求完成实验方案一和实验方案二(下表中“实验结论”填“=”“>”或“<”)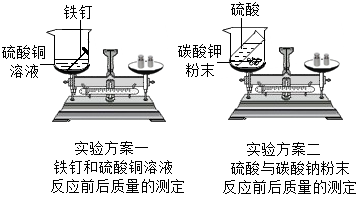
| 实验方案 | 实验一 | 实验二 |
| 反应现象 | 铁钉表面覆盖一层红色的物质,溶液由蓝色变成浅绿色 | 有气泡产生 |
| 化学方程式 | Fe+CuSO4=FeSO4+Cu | H2SO4+K2CO3═K2SO4+CO2↑+H2O |
| 反应前的总质量 | m1 | n1 |
| 反应后的总质量 | m2 | n2 |
| 实验结论 | m1= m2 | n1> n2 |
分析 化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和;
化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答 解:铁和硫酸铜反应生成硫酸亚铁和铜,铁钉表面覆盖一层红色的物质,溶液由蓝色变成浅绿色,反应的化学方程式为:Fe+CuSO4=FeSO4+Cu,反应前后质量相等,即m1=m2;
碳酸钾和稀硫酸反应生成硫酸钾、水和二氧化碳,反应的化学方程式为:H2SO4+K2CO3═K2SO4+CO2↑+H2O,反应过程中产生大量气泡,生成的二氧化碳逸出装置外,因此n1>n2,实验过程如下表所示:
| 实验方案 | 实验一 | 实验二 |
| 反应现象 | 铁钉表面覆盖一层红色的物质,溶液由蓝色变成浅绿色 | 有气泡产生 |
| 化学方程式 | Fe+CuSO4=FeSO4+Cu | H2SO4+K2CO3═K2SO4+CO2↑+H2O |
| 反应前的总质量 | m1 | n1 |
| 反应后的总质量 | m2 | n2 |
| 实验结论 | m1=m2 | n1>n2 |
故填:碳酸钾粉末与硫酸反应产生的气体逸出;使反应在密闭容器中进行.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
相关题目
4. 碳和部分碳的化合物间转化关系如图所示.下列说法中错误的是( )
碳和部分碳的化合物间转化关系如图所示.下列说法中错误的是( )
 碳和部分碳的化合物间转化关系如图所示.下列说法中错误的是( )
碳和部分碳的化合物间转化关系如图所示.下列说法中错误的是( )| A. | 固态X俗名叫“干冰”,常用作制冷剂 | |
| B. | H2CO3能紫色石蕊溶液变成红色,说明X具有酸性 | |
| C. | 反应2CuO+C $\frac{\underline{\;高温\;}}{\;}$ 2Cu+X↑体现了碳的还原性 | |
| D. | X转化为CO的反应为X+C$\frac{\underline{\;高温\;}}{\;}$2CO |
2.下列方法能使海水转化为饮用水的是( )
| A. | 过滤 | B. | 吸附 | C. | 搅拌 | D. | 蒸馏 |
9.60℃时,某物质在20克水中,最多溶解0.8克,则该物质的溶解性为( )
| A. | 可溶 | B. | 易溶 | C. | 微溶 | D. | 无法确定 |
19.玻璃棒是化学实验的常用仪器,下列实验过程中不需要使用玻璃棒的是( )
| A. | 稀释浓硫酸 | B. | 用量筒量取一定体积的水 | ||
| C. | 蒸发氯化钠溶液 | D. | 除去悬浮在河水中的不溶物 |
6.下列各组物质的溶液,不用其他试剂,只用观察以及用组内物质的溶液相互混合的方法,就能将他们鉴别出来的是( )
| A. | NaCl BaCl2 CuSO4 NaOH KNO3 | |
| B. | Ba(NO3)2 NaCl Na2SO4 H2SO4 HCl | |
| C. | NaOH FeCl3 MgSO4 BaCl2 KCl | |
| D. | AgNO3 HCl Na2CO3 KCl NaCl |
3.2016年6月5日是世界环境日,主题是“为生命呐喊”,与之相呼应的中国主题为“改善环境质量,推动绿色发展”.下列做法不符合这一主题的是( )
| A. | 购物时用布袋代替塑料袋 | B. | 农田大量施用农药、化肥 | ||
| C. | 工业废水经处理后再排放 | D. | 推广使用节能灯和太阳能路灯 |
4.下列方程式合理的是( )
| A. | Cu+FeCl2=Fe+CuCl2 | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | Ca(OH)2+Na2CO3=CaCO3↓+2NaOH | D. | K2SO4+CuCl2=CuSO4+2KCl |