题目内容
4.下列方程式合理的是( )| A. | Cu+FeCl2=Fe+CuCl2 | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | Ca(OH)2+Na2CO3=CaCO3↓+2NaOH | D. | K2SO4+CuCl2=CuSO4+2KCl |
分析 根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
解答 解:A、在金属活动顺序表中,铜排在铁的后面,不能置换铁盐中的铁,故选项错误;
B、铁在氧气中燃烧生成四氧化三铁,正确的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
C、该化学方程式完全正确.
D、生成物中没有气体、沉淀或水生成,故反应不能发生.
故选:C
点评 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.

练习册系列答案
相关题目
14.请回忆你学习过程的“质量守恒定律”的实验探究,并按要求完成实验方案一和实验方案二(下表中“实验结论”填“=”“>”或“<”)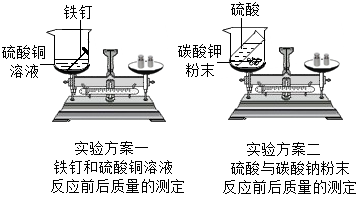
将两个实验结果进行讨论对比时,有同学分析:有一个方案观察到天平不平衡,是因为碳酸钾粉末与硫酸反应产生的气体逸出,因此不能说质量不守恒,在反应物不变的前提下,要使天平平衡,你对该方案的改进措施是使反应在密闭容器中进行.

| 实验方案 | 实验一 | 实验二 |
| 反应现象 | 铁钉表面覆盖一层红色的物质,溶液由蓝色变成浅绿色 | 有气泡产生 |
| 化学方程式 | Fe+CuSO4=FeSO4+Cu | H2SO4+K2CO3═K2SO4+CO2↑+H2O |
| 反应前的总质量 | m1 | n1 |
| 反应后的总质量 | m2 | n2 |
| 实验结论 | m1= m2 | n1> n2 |
15.下列过程中,一定发生化学变化的是( )
| A. | 酒精燃烧 | B. | 水结成冰 | C. | 汽油挥发 | D. | 玻璃破碎 |
12.水是我们日常生活中必不可少的物质,下列有关水的说法正确的是( )
| A. | 可用肥皂水区分硬水和软水 | |
| B. | 用过滤的方法可以使硬水软化 | |
| C. | 活性炭吸附水中的异味和色素是化学变化 | |
| D. | 水通电分解时产生的氢气和氧气质量比为2:1 |
19.化学与生产、生活、社会息息相关,下列说法错误的是( )
| A. | 胃酸过多的人应少饮葡萄汁(葡萄汁的pH为3.4-4.5) | |
| B. | 人体缺锌会引起生长发育缓慢,但锌元素并不是摄入得越多越好 | |
| C. | 为了个人卫生,应全部使用一次性的木筷和餐盒 | |
| D. | 多用电子邮件、MSN、QQ等即时通讯工具,少用传真打印等属“低碳”方式 |
9.经测定,在任何水溶液中,均存在一定数量的H+【用n(H+)表示】和一定数量的OH-【用n(OH-)表示】,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:
据此分析
(1)常温下测得水中pH=7,可知水中n(H+)=n(OH-)(填“>”或“=”或“<”,下同).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,原因是该溶液中n(H+)<n(OH-).
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)>n(OH-).
(4)通过上述信息,由此得出盐溶液一定显中性是否正确?错误(填“正确”或“错误”).
| n(H+)与n(OH-)的相对大小 | 溶液的酸碱性 |
| n(H+)>n(OH-) | 酸性 |
| n(H+)=n(OH-) | 中性 |
| n(H+)<n(OH-) | 碱性 |
(1)常温下测得水中pH=7,可知水中n(H+)=n(OH-)(填“>”或“=”或“<”,下同).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,原因是该溶液中n(H+)<n(OH-).
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)>n(OH-).
(4)通过上述信息,由此得出盐溶液一定显中性是否正确?错误(填“正确”或“错误”).
13.如图是某反应的微观示意图.下列说法正确的是( )

| A. | 该反应生成物有三种 | |
| B. | 该反应属于置换反应 | |
| C. | 反应前后分子的个数没有改变 | |
| D. | 该反应中H2S与O2的分子个数比为2:3 |